ОСОБЕННОСТИ ЭКСТРАКЦИИ ЙОДА ИЗ ПРЕПАРАТА «ЛЮГОЛЬ С ГЛИЦЕРИНОМ»
Секция: 4. Медицинские науки

XXIII Студенческая международная заочная научно-практическая конференция «Молодежный научный форум: естественные и медицинские науки»
ОСОБЕННОСТИ ЭКСТРАКЦИИ ЙОДА ИЗ ПРЕПАРАТА «ЛЮГОЛЬ С ГЛИЦЕРИНОМ»
Актуальность.
1. Йодированное масло применяется там, где эндемия йодной недостаточности выражена в средней или высокой степени.
2. Преимущество йодированного масла в сравнении с йодированной солью состоит в собственной энергетической и пищевой ценности: масло богато жирными ненасыщенными кислотами.
3. Кроме того, растительное масло, в отличие от соли, не нуждается в жестком контроле его потребления при риске или наличии сердечно-сосудистых заболеваний.
Экспериментальная часть.
Состав препарата «Люголь» с глицерином: 1 г йода, 2 г йодида калия, 94 г глицерина, 3 г воды. Столовое растительное масло (подсолнечное и кукурузное) использовали в качестве экстрагента процесса экстракции йода из аптечного препарата.
Для проведения экстракции готовили композиции по методу переменных объемов [3, с. 419], содержащие 2, 4, 6, 8 мл препарата «Люголь» и дистиллированную воду, а также композиции, в которых 10 мл воды заменили на глицерин. Количество масла для экстракции — 8, 10, 12 и 14 мл. Общий объем композиции составлял 50 мл.
Определение коэффициентов распределения йода (К) в системах (вода) — (столовое растительное масло) и (глицерин — вода) — (столовое растительное масло) проводили в делительной воронке. Установление равновесия констатировали по воспроизводимости результатов титрования водной фазы раствором тиосульфата натрия через различные промежутки времени (2, 5, 10 мин). После установления равновесия отбирали пробы из водного слоя и определяли концентрацию йода титрованием 0,01 М раствором тиосульфата натрия. Равновесную концентрацию йода в органической (масляной) фазе рассчитывали по разности исходной концентрации йода и его концентрации в водной фазе после расслоения и использовали для дальнейшего вычисления коэффициента распределения К [3, с. 419].
В данной работе один из растворителей — вода, в которой плохо растворяется йод, а другой — органический растворитель (столовое растительное масло). В нем йод растворяется хорошо. Изучение равновесия производили при комнатной температуре.
Равновесие некоторых химических реакций (диссоциация на ионы, ассоциация молекул и др.) в растворах можно изучить, исследуя распределение растворенного вещества между двумя несмешивающимися жидкостями. Воспользуемся формулой Шилова:
![]() , (1)
, (1)
где: КТ — коэффициент распределения при заданной Т; ![]() — концентрация йода в масле; п — степень полимеризации молекул йода в воде;
— концентрация йода в масле; п — степень полимеризации молекул йода в воде; ![]() — концентрация йода в воде.
— концентрация йода в воде.
Логарифмируя уравнение (1), получаем:
![]() . (2)
. (2)
После преобразования получаем выражение:
![]() . (3)
. (3)
Уравнение (3) является математическим описанием прямой линии вида:
у = а + bх, где ![]() ,
, ![]() , b=n,
, b=n, ![]() . (4)
. (4)
В равновесии 2I-(вода) « I2(масло)
коэффициент распределения К рассчитывали по эмпирической формуле:
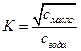 (5)
(5)
Значение коэффициента распределения йода, рассчитанное по уравнению (5) составило 118.
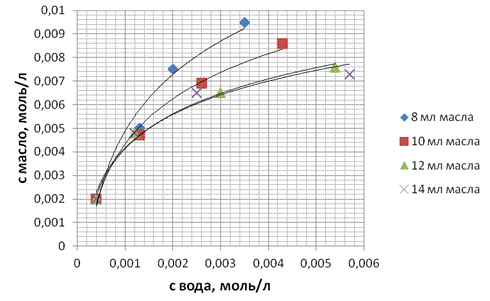
Рисунок 1. Изотермы экстракции йода различными объемами экстрагента (экстрагент — подсолнечное масло)
Необходимо отметить тот факт, что экспериментальные зависимости являются логарифмическими (в отличие от представленных в [3, с. 419] линейных) и адекватно описываются уравнениями с коэффициентами аппроксимации 96—99 %.
Равновесие I2(водн) ↔ I2(органич.) смещено в сторону распределения в органическую фазу (масло). Однако, при увеличении содержания йода в исходных композициях коэффициент распределения заметно уменьшается.
Та же динамика наблюдается при увеличении объема экстрагента (масла). Это хорошо видно из представленных на рис. 1 изотерм. Причем большое количество масла в композиции при предварительном встряхивании приводит к образованию стойкой эмульсии.

Рисунок 2. Изотермы экстракции в логарифмических координатах (экстрагент — подсолнечное масло)
Входящий в состав препарата йодид калия улучшает растворение йода в воде, так как реакция идет с образованием KI3, хорошо растворимого в воде: I2 + KI = KI3 [2, с. 76]. Однако, при добавлении к композициям глицерина, извлечение компонента маслом уменьшается.

Рисунок 3. Изотермы экстракции при замене 10 мл воды глицерином
Это связано с меньшей полярностью глицерина по сравнению с водой (по данным HyperChem дипольный момент для воды — 1,365, для глицерина — 1,075 (рассчитано, исходя из принципа молекулярной динамики)). Это приводит к большей растворимости йода в рассмотренных композициях, но к худшему его экстрагированию.
Во-вторых, в реакции с йодистым водородом могут быть замещены все гидроксильные группы глицерина, но образующийся при этом трийодпропан восстанавливается йодистым водородом в йодистый изопропил:

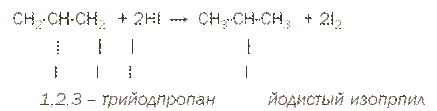
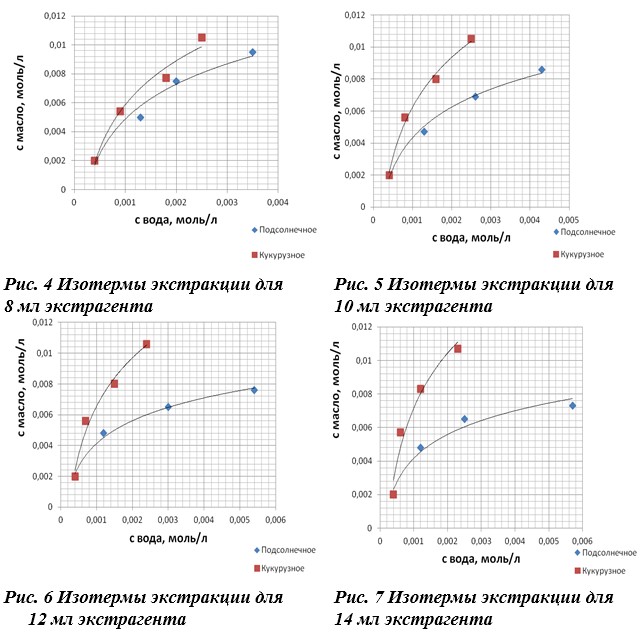
На рис. 4—7 представлены для сравнения изотермы экстракции йода подсолнечным и кукурузным маслом. В табл. 1 представлен приблизительный состав основных триглицеридов некоторых природных масел [1, с. 228].
Таблица 1.
Приблизительный состав основных триглицеридов природных масел
Масло |
Высшие жирные кислоты (ВЖК), масс.доля, % |
|||||
Миристи- |
Пальмити- |
Стеари- |
Олеиновая |
Линолевая |
Линоленовая |
|
Подсолнечное масло |
|
11 |
4 |
38 |
46 |
|
Кукурузное масло |
2 |
10 |
3 |
34 |
51 |
|
Льняное масло |
|
5 |
3 |
5 |
62 |
25 |
Оливковое масло |
|
10 |
2 |
82 |
4 |
|
Заключение.
1. По предварительной оценке, эффективность экстракции йода из йодсодержащих фармацевтических препаратов при использовании в качестве экстрагента растительного масла напрямую зависит от концентрации ненысыщенных высших жирных кислот (НВЖК). На это указывает, в частности, увеличение коэффициента распределения йода между органической фазой (маслом) и водой при прочих равных условиях.
2. Динамика изменения концентрации йода при увеличении количества экстрагента зависит не только от общего содержания НВЖК, но и от иных факторов (процентный состав НВЖК, степень очистки и т. д.).
Список литературы:
1. Артеменко А.И. Органическая химия. — М.: Высш. шк., 2000. — 536 с.
2. Герасимова Галина Викторовна. Фазовые равновесия в тройных и четверных иодсодержащих системах: Дис. ... канд. хим. наук: 02.00.04.: Саратов, 2004, 243 c.
3. Пономарева П.А. Определение термодинамических параметров экстракции йода ТБФ в смеси с изооктаном из высокоминерализованных растворов / Вестник ОГУ № 12 (131). — 2011. — С. 419—420.





