ЭТИОЛОГИЯ И МЕТОДЫ ДИАГНОСТИКИ ЦЕРЕБРАЛЬНОЙ АУТОСОМНО-ДОМИНАНТНОЙ АРТЕРИОПАТИИ С СУБКОРТИКАЛЬНЫМИ ИНФАРКТАМИ И ЛЕЙКОЭНЦЕФАЛОПАТИЕЙ
Секция: 4. Медицинские науки

XXIII Студенческая международная заочная научно-практическая конференция «Молодежный научный форум: естественные и медицинские науки»
ЭТИОЛОГИЯ И МЕТОДЫ ДИАГНОСТИКИ ЦЕРЕБРАЛЬНОЙ АУТОСОМНО-ДОМИНАНТНОЙ АРТЕРИОПАТИИ С СУБКОРТИКАЛЬНЫМИ ИНФАРКТАМИ И ЛЕЙКОЭНЦЕФАЛОПАТИЕЙ
CADASIL (cerebral autosomal dominant arteriopathy with subcortical infarcts and leukoencephalopathy) — церебральная аутосомно-доминантная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией является наиболее частой наследственной причиной инсульта и сосудистой деменции у людей среднего возраста. У пациентов наблюдается увеличение частоты возникновения мигреней с аурой. МРТ-исследования часто выявляют изменчивую картину ишемии белого вещества головного мозга.
Генетические исследования установили, что основополагающей причиной возникновения CADASIL является мутация в гене Notch3 (19 — я хромосома).
В норме гены группы Notch кодируют трансмембранные рецепторы, участвующие в дифференцировке клеток в процессе онтогенеза. В 95 % случаев при CADASIL выявляются миссенс-мутации в этом гене, следствием которых является потеря, либо наращивание цистеинового остатка определенного домена трансмембранного белка. В результате происходит изменение третичной структуры белка, а, следовательно, и нарушение его функции.
Клиническая картина.
CADASIL в клинической практике характеризуется пятью основными симптомами:
1. Мигренозоподобная головная боль с аурой, встречающаяся у 20—40 % пациентов, а также мигрень без ауры, которая сочетается с вышеназванной;
2. Транзиторная ишемическая атака подкорковых отделов головного мозга;
3. Ишемический инсульт;
4. Деменция лобно-подкоркового характера;
5. Когнитивные нарушения.
Каждый из пяти основных симптомов может проявляться изолированно или в совокупности с остальными.
Мигренозоподобные головные боли при CADASIL возникают у людей в среднем возрасте около 30 лет. Для женщин это — 26 лет, а для мужчин — 36. Очень часто ранний возраст, в котором возникают боли, коррелирует с высокой концентрацией гомоцистеина в сыворотке крови.
Мигренозные атаки, длящиеся 20—30 минут, у большинства пациентов предваряются появлением визуальной или звуковой ауры. Которая, в последствии, сменяется сильнейшей головной болью, длящейся несколько часов.
Однако у 38 % пациентов наблюдались атипичные формы приступов мигрени, такие как: гемиплегическая (при которой появляется повторяющаяся временная слабость с одной стороны тела), базилярная (характеризуется снижением уровня сознания, двусторонними парезами).
Транзиторные ишемические атаки, а также ишемические инсульты являются наиболее частыми проявлениями CADASIL, выявляемые у 60—85 % пациентов. Средний их возраст составляет, в ряде случаев, 49 лет (в диапазоне от 20 до 70 лет). Довольно часто у пациентов не наблюдалось ранее предрасполагающих заболеваний сосудов головного мозга (атеросклероз и тромбообразование; кардиогенная эмболия (20 % случаев); стеноз прецеребральных и церебральных артерий), являющихся первопричинами подобных нарушений.
Впрочем, у 20 % была диагностирована гипертензия, а также высокий уровень холестерина в крови. У 50 % пациентов в крови был обнаружен никотин.
Ишемические нарушения в 67 % случаев представлены лакунарным инсультом.
Лакунарный инсульт — одно из видов ишемических нарушений кровообращения головного мозга. Возникает, как правило, при артериальной гипертензии, характеризующейся развитием не очень больших очагов некроза, которые, в дальнейшем, преобразуются в лакуны, локализующиеся в глубинных отделах головного мозга. Происходит поражение перфорирующих артерий, вследствие чего лакунарные инсульты никогда не затрагивают кору больших полушарий.

Рисунок 1. Локализация лакунарного инфаркта головного мозга
Существуют различные разновидности лакунарных синдромов:
1. Изолированный двигательный гемипарез (около 50 % случаев) — односторонняя слабость, охватывающая несколько отделов тела;
2. Изолированная гемианестезия (около 5 % случаев) — локализованное нарушение всех видов чувствительности;
3. Атактический гемипарез (10 % случаев);
4. Изолированный центральный паралич мышц лица, синдром дизартрии и неловкой руки.
Большинство пациентов перенесли от двух до пяти рецидивирующих инсультов за год. В дальнейшем это привело к нарушению координации, псевдобульбарному параличу.
Также у пациентов отмечалось снижение уровня настроения, вплоть до апатии; депрессивное состояние, утрата мотивации, ухудшения когнитивного восприятия, а также нарушение исполнительных функций, несвязанных с депрессией были признаны основным клиническим проявлением CADASIL, отмеченным у 40 % пациентов.
Среди иных клинических проявлений отмечались также внутримозговые кровоизлияния (единичные случаи), глухота, слепота, паркинсонизм.
Одной из особенностей CADASIL является отсутствие симптоматических проявлений относительно других органов, помимо мозга. Исключение составляет инфаркт миокарда.
Методы диагностики.
Лакунарные инсульты и лейкоэнцефалопатии лучше всего обнаруживаются путем использования МРТ. У всех пациентов с CADASIL-синдромом обнаруживается лейкоареоз (в режиме МРТ — Т1) в области височных долей, который является основным нейровизуализационным маркером.
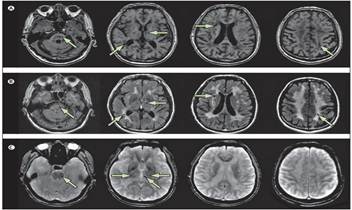
Рисунок 2. Основные нейровизуализационные маркеры (снимок МРТ, режим Т1)
Лейкоареоз, иначе говоря, «паравентрикулярное свечение» — это диффузное двустороннее изменение белого вещества полушарий головного мозга в виде снижения его плотности, чаще всего вокруг боковых желудочков.
Выделяют два типа лейкоареоза:
1. Паравентрикулярный (в виде «полоски» охватывает боковые желудочки головного мозга по периметру, либо с стороны переднего или же заднего полюса);
2. Субкортикальный (локализованные, рассеянные небольшого размера очаги в глубинных отделах больших полушарий, не исключая семиовальный центр).
Субкортикальный лейкоареоз, который охватывает область наружной капсулы, выявляется у 65 % больных на ранних стадиях заболевания. Лейкоэнцефалопатия и подкорковые инфаркты определяются у 75 % пациентов.
Довольно часто у пациентов с CADASIL-синдромом отсутствуют очаговые поражения головного мозга, а также клинические проявления заболевания.
Тем не менее, МРТ в режиме Т2 позволяет диагностировать наличие отёков, глиоза, демиелинизации нервных волокон головного мозга. Выявление подобных изменений весьма важно для правильной постановки диагноза.

Рисунок 3. Наличие отеков и демиелинизации. Снимок МРТ (в режиме Т2)
Базальные ганглии и таламус также поражаются при CADASIL-синдроме (коренное отличие данного заболевания от рассеянного склероза!).
Лакунарные инфаркты различной формы, размера и численности проявляются на T1 — взвешенных изображениях в точечных, либо вытянутых областей пониженного сигнала.
Диффузионно-взвешенная МРТ может показать небольшие участки повышенного сигнала, что во многих случаях свидетельствует о недавно произошедших микроинфарктах. Среди иных находок можно отметить расширенные периваскулярные пространства в области базальных ядер.
Микрокровоизлияния обнаруживаются у 25—69 % пациентов (T2 — режим МРТ); с возрастом частота этих процессов только увеличивается. Этому способствует повышение артериального давления, часто обусловленное повышением концентрации гемоглобина и альбуминов в крови.
Исследования показывают, что у пациентов с CADASIL-синдромом атрофия головного мозга прогрессирует в три раза быстрее, чем у здоровых людей в результате процесса старения. Скорость атрофии может коррелировать в зависимости от объема лакунарных очагов.
Также, применяется биопсия кожи. Это самый простой метод подтверждения диагноза CADASIL. Электронно-микроскопические исследования выявляют специфические гранулярные осмиофильные включения среди дегенерировавших миоцитов стенки артериол дермы кожи. Считается, что белок Notch3 является одним из компонентов этих гранул. Их накопление, а также дегенерация гладких миоцитов стенок сосудов при CADASIL-cиндроме инициируются довольно рано, обнаружить это возможно у пациентов в возрасте до 20 лет.
Генетика и патогенез.
При макроскопическом осмотре головного мозга обнаруживаются изменения, типичные для хронических заболеваний мелких сосудов:
· Диффузная бледность миелина;
· Множественные разрежения в области белого вещества (в основном, перивентрикулярная зона и семиовальный центр);
· Расширения пространств Робина-Вирхова.
В корковом веществе также был обнаружен распространенный нейрональный апоптоз (преимущественно в пирамидном и ганглионарном слоях). Область поражения увеличивается вследствие обширного ишемического поражения подкорковых образований.
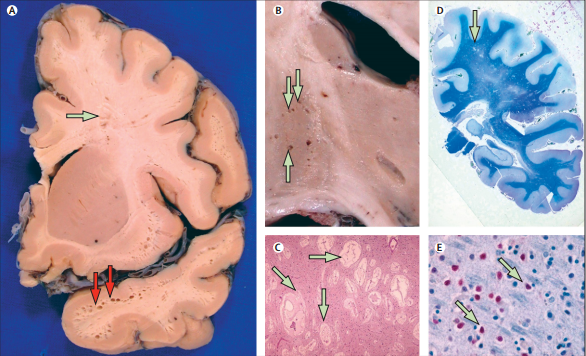
Рисунок 4. Патологические признаки ишемического поражения головного мозга
Микроскопические и ультраструктурные исследования демонстрируют специфическую артериопатию, затрагивающую в основном небольшие пенетрирующие и лептоменингиальные церебральные артерии. В данном случае, артериопатия характеризуется утолщением артериальных стенок, сужением просвета артерий и стенозом эндотелия. Причиной этих изменений является накопление в околоклеточном пространстве близ плазмолемм гладких миоцитов осмиофильных гранул.
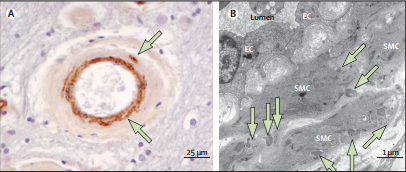
Рисунок 5. Микроскопические и ультраструктурные исследования артериальных поражений головного мозга
Молекулярная генетика.
CADASIL-синдром — аутосомно-доминантное заболевание, вызванное, как говорилось в начале, мутациями в гене Notch3, расположенном на 19-й хромосоме и кодирующем трансмембранный рецептор, имеющий отношение к сигнальным путям контроля клеточного цикла и развития.

Рисунок 6. Схема трансмембранного рецептора, кодируемого геном Notch3; его мутации
Сам рецептор состоит из 2321 аминокислоты, содержит в своем составе 34 повтора (EGFR), в каждом из которых содержится шесть остатков цистеина; три узкополосных повтора, одиночный трансмембранный и внутриклеточный домены. Последний содержит семь анкириновых (ANKR) повторов.
В составе гена Notch3 имеется 33 экзона. Мутации затрагивают, в основном, от 2 до 24 экзонов. Они кодируют все 34 повтора EGFR. Сильная кластеризация затрагивает экзоны 3 и 4, которые кодируют 2—5 EGFR (>40% мутаций происходят именно в этих экзонах).
Практически 95 % всех мутаций являются миссенс-мутациями. На оставшиеся 5 % приходятся мутации, обусловленные сдвигом рамки считывания, а также делеции.
Мутагенез приводит к возникновению нечетного количества остатков цистеина в пределах внеклеточного домена EGFR.
На трансгенных моделях показано, что дисфункция Notch3 ведет к нарушению цереброваскулярной реактивности и повышению резистентности церебральных сосудов.
Механизмы, лежащие в основе симптоматики CADASIL-синдрома.
Различные исследования с применением однофотонной эмиссионной КТ, ПЭТ, МРТ показывают, что ранее снижение уровня кровоснабжения, и как следствие, метаболизма, позволяют предположить наличие ишемических подкорковых нарушений. Нарушение церебральной гемодинамики, вероятно, возникает в результате структурных и функциональных изменений в церебральных артериях. Патологоанатомические исследования выявили стеноз мелких артерий и артериол, располагающихся в белом веществе головного мозга. У пациентов также отмечалась вазореактивность на фоне фиброза и дегенерации гладких миоцитов артериальных стенок.
Лечение.
На данный момент не существует общепризнанных методов лечения данного заболевания. Большинство специалистов рекомендуют принимать аспирин в малых дозах, а также другие статины и антиагреганты, которые участвуют в регуляции функций эндотелия. Пентоксифиллин часто используется для улучшения микроциркуляции в головном мозге.
Антикоагулянты абсолютно противопоказаны, поскольку их применение может повлечь за собой развитие геморрагического инсульта.
Симптоматическое лечение мигрени проводится по общепринятым схемам. Возникающие расстройства эмоционального характера устраняются назначением для приема седативных препаратов, а также антидепрессантов.
Вывод: своевременное диагностирование CADASIL, а также тождественных генетических синдромов, позволяет расширить актуальные представления о патогенетической гетерогенности ишемических нарушений кровообращения головного мозга. Внедрение новейших фармокологических методов ангио- и нейропротекции в медицинскую практику, позволит проводить превентивную терапию для новоявленных клинически здоровых лиц, находящихся в «группе риска» и предотвращать у них возможное возникновение данного заболевания.
Список литературы:
1. Буссер М.Г., Жутель А., Шабриа Х. и др. ЦАДАСИЛ — церебральная аутосомно-доминантная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией. Неврол. журн. 1997; 3: 20—25.
2. Грин Н., Стау У., Тейлор Д. Биология. — 2010. — С. 237—245.
3. Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция. — М., 2002.
4. Мозолевский Ю.В., Янакаева Т.А., Мельникова Е.А. и др. Церебральная аутосомно-доминантная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией. Неврол. журн. 2005; 2: 34—40.
5. Kalimo H., Ruchoux M., Viitanen M. еt. al. CADASIL: a common form of hereditary arteriopathy causing brain infarcts and dementia. Brain Pathol. 2002; 12: 371—384.





