ТЕЛОМЕРЫ И КАНЦЕРОГЕНЕЗ: АНАЛИЗ СОВРЕМЕННЫХ ИССЛЕДОВАНИЙ И ПЕРСПЕКТИВЫ ПРАКТИЧЕСКОГО ПРИМЕНЕНИЯ МЕТОДОВ
Секция: 2. Биологические науки

XXIV Студенческая международная заочная научно-практическая конференция «Молодежный научный форум: естественные и медицинские науки»
ТЕЛОМЕРЫ И КАНЦЕРОГЕНЕЗ: АНАЛИЗ СОВРЕМЕННЫХ ИССЛЕДОВАНИЙ И ПЕРСПЕКТИВЫ ПРАКТИЧЕСКОГО ПРИМЕНЕНИЯ МЕТОДОВ
Целью данной публикации является анализ современных работ в области контроля роста и развития теломерных участков хромосом, а также исследований, посвященных взаимосвязи активности теломер и канцерогенеза.
Известно, что при делении клеток теломеры уменьшаются, защищая кодирующие части ДНК хромосом, поскольку фермент, который копирует ДНК, не дочитывает её крайние нуклеотиды. Однако, теломеры не безразмерны, поэтому и клетка может делиться ограниченное количество раз. Это число называется пределом Хейфлика и примерно равно 50. Когда клетка достигает этого предела, она погибает вследствие неизбежных повреждений в белковых молекулах и ДНК. В связи с этим была выдвинута гипотеза о том, что искусственное удлинение теломер может способствовать замедлению процессов старения [4, c. 585]. Существует естественный способ удлинения теломер — за счет действия фермента теломераза. Это фермент, добавляющий особые повторяющиеся последовательности к 3' концу ДНК на концах хромосом.
Так как теломераза активна только в стволовых клетках и гаметах, ученые разрабатывают различные технологии по увеличению теломер и в обычных соматических клетках, которые будут способны излечить различные генетические заболевания.
Разработкой подобной технологии занимались ученые из Стэнфордского университета [5, c. 1933]. Исследователи провели эксперимент, в ходе которого культивировали человеческие клетки и увеличили их концевые участки хромосом. В ходе исследования основная группа клеток много дольше вела себя как молодая, размножаясь внутри чашки Петри, в то время как у контрольной группы, которая не подвергалась модиикации, жизненные функции быстро начали угасать. Основным действующим компонентом данной методики является измененная РНК, которая переносит инструкции из генов ДНК в белковые фабрики клеток. РНК из этого эксперимента содержит последовательность, кодирующую каталитическую субъединицу TERT (telomerase reverse transcriptase) — которая является активным компонентом природного фермента теломеразы.
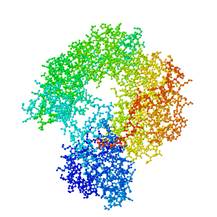
Рисунок 1. Структура каталитической субъединицы теломеразы TERT (илл. из: http: //learn.genetics.utah.edu/content/chromosomes/te.)
Данная технология имеет огромное преимущество перед другими потенциальными методами — модифицированная РНК исчезает уже через 48 часов, по истечении которых теломеры снова начинают укорачиваться с каждым новым делением. Поясним, почему данный эфффект является плюсом. Если данная методика не была бы временной, теломеры бы постоянно увеличивались, клетка бы не достигала предела Хейфлика и делилась бы бесконечно и бесконтрольно, что как уже упоминалось в начале работы, является огромным риском канцерогенеза. Ученые сообщают, что на данный момент, эта технология направлена на излечение генетических заболеваний. К примеру, при мышечной дистрофии Дюшена длина теломер в мышечных клетках значительно меньше чем у контрольной группы. Так, при помощи этой технологии, ученые смогут выращивать дополнительные мышцы с удлиненными концевыми участками хромосом, которые помогут вылечить данное заболевание [6, c. 1059]. В дальнейшем данная технология может быть применена для использования в комплексе мероприятий по увеличению продолжительности жизни здоровых людей.
На данный момент существует единственный потенциально возможный способ удлинения теломер без медицинского вмешательства. Это ведение здорового образа жизни. Данный вывод можно сделать на основе результатов оригинальных работ, одной из которых является исследование Дина Орниша. Необходимо отметить, что данное исследование являлось пилотным.
В течении 5 лет проводились наблюдения за 35 мужчинами с начальной стадией рака простаты (карцинома предстательной железы). Десять участников эксперимента на время наблюдения кардинально изменили свой образ жизни. Они перешли на диету, основными продуктами питания в которой были овощи, фрукты и цельные злаки. Также было снижено потребление жиров и простых углеводов. Регулярно они совершали кратковременные прогулки на свежем воздухе и боролись со стрессом, посредством медитации, йоги и дыхательных упражнений. Также проводились групповые занятия с целью облегчить их переход к новому образу жизни. В течении всего эксперимента осуществлялисьь наблюдения за изменением длин теломер у всех испытуемых.
Таблица 1.
Компоненты здорового образа жизни
Питание |
Повышенное количество растительного белка, фруктов, овощей. Низкое содержание жиров (10 % от общего количества калорий) и простых углеводов. |
Упражнения |
Умеренные аэробные нагрузки — 30 минутная прогулки в течение 6 дней в неделю. |
Управление стрессом |
Элементы йоги, дыхательные упражнения и медитация. |
Социальная поддержка |
Раз в неделю проводятся групповые занятия по снятию стресса |
Исследование показало, что теломеры участников эксперимента удлинились примерно на 10 %. Стоит подчеркнуть, что речь идет именно об удлинении теломер, а не о снижении скорости их укорочения. Также была выявлена прямая зависимость между соблюдением рекомендаций по здоровому образу жизни и процессом удлинения теломер. Теломеры контрольной группы стабильно укорачивались и к концу эксперимента это сокращение составило примерно 3 %.
При этом следует отметить, что данное исследование не является полноценным в силу малого объема выборки и может служить лишь иллюстрацией возможной зависимости между длиной и функциональной активностью теломер и образом жизни человека. Кроме того, мы полагаем, что работа Орниша лишний раз иллюстрирует влияние стресса на здоровье человека.
На основании проанализированных нами работ, можно попытаться понять, существует ли доказанная опытным путем, связь между протяженность теломер (короткие теломеры) и возникновением злокачественных новообразований.
Многочисленные исследования подтверждают факт того, что у людей с короткими теломерами повышен риск развития онкологических заболеваний. Так, у пациентов с врожденным дискератозом (генетическим заболеванием, при котором в хромосомах человека наблюдаются укороченные теломеры), повышен риск развития рака, в особенности рака языка (в 1000 раз), острой миелоидной лейкемии (в 200 раз), а также плоскоклеточной карциномы головы и шеи.
При отдельных заболеваниях, укороченные теломеры уже давно считаются прогностическим фактором развития онкологии. Так, короткие концевые участки хромосом являются сигналом к прогрессии хронических воспалительных состояний со стороны желудочно-кишечного тракта в злокачественные заболевания: апластическая анемия прогрессирует в миелодиспластический синдром или острую миелоидную лейкемию, воспалительная болезнь кишечника — в рак толстого кишечника, а синдром Баретта — в аденокарциному [3, c. 1439]. Также результаты множества полногеномных ассоциативных исследований показали, что локус TERT является значимым локусом предрасположенности к различным типам рака, однако с относительно низкими уровнями вероятности.

Рисунок 2. График зависимости риска возникновения рака от уменьшения теломер (http://f1000.com/prime/reports/m/4/8)
Связь между длинными теломерами и канцерогенезом представляеся теоретической, поскольку на данный момент не имеется никаких технологий, способных удлинить теломеры настолько, чтобы клетка делилась беспрерывно и бесконтрольно. Даже в самих раковых клетках активная работа теломеразы не успевает за тем огромным количеством делений, что происходят. По этой причине длина теломер все равно остается на относительно низком уровне.
Однако, длина теломер может изменяться естественным путем, с течением времени. У людей пожилого возраста длина теломер существенно меньше чем у более молодых.

Рисунок 3. Зависимость длины теломер от возраста человека
В заключении мы хотим отметить, что на данный момент взаимосвязь между длиной теломер и канцерогенезом до конца не установлена. Кроме того, можно предположить, что фактор стресса способен оказывать устойчивое влияние на структуру и функциальные возможности теломер, однако, вектор влияния стресса (негативное или позитивное) на теломеры — также является предметом новых полноценных исследований.
Список литературы:
1. Анисимов В.Н., 2008. Теории и модели старения и смертности // Молекулярные и физиологические механизмы старения. Спб «Наука» 2008. 481 с.
2. Галицкий В.А. Эпигенетическая природа старения // Цитология Том 51, № 5. 2009. С. 388—397.
3. Alter B.P., Baerlocher G.M. Very short telomere length by flow fluorescence in situ hybridization identifies patients with dyskeratosis congenita. NCBI Р. 1439—47. April. 2007.
4. Hayflick L., Moorhead P.S. The serial cultivation of human diploid cell strains // Experimental cell research 25. Р. 585—621; 1961.
5. Helen M. Blau, John P. Cooke, Juan G. Santiago. TheFACEB Journal vol. 29 no. 5 Р. 1930—1939 31, 2014.
6. Prof Dean Ornish. The Lancet Oncology Journal Volume 14, № 11, Р. 1112—1120. September 2013.
7. Socco A. Short telomeres and stem cell exhaustion model Duchenne muscular dystrophy in mdx/mTR mice. NCBI. Р. 1059—71. December 2010.
8. Telomere Length and risk of incident Cancer and Cancer Mortality Jama Journal Vol 304, № 1 Р. 69—75. July 2010.
9. Укорочение теломер и рак — [Электронный ресурс] — Режим доступа. — URL: http://www.vechnayamolodost.ru/pages/teoriistarenija/teloiboldb.html (Дата обращения 01.05.2015).
10. Learn.genetics — [Электронный ресурс] — Режим доступа. — URL: http://learn.genetics.utah.edu/content/chromosomes/telomeres/ (Дата обращения 04.05.2015).





