ПРЕНАТАЛЬНАЯ ДИАГНОСТИКА РЕДКИХ ХРОМОСОМНЫХ ЗАБОЛЕВАНИЙ
Секция: 4. Медицинские науки

XXIV Студенческая международная заочная научно-практическая конференция «Молодежный научный форум: естественные и медицинские науки»
ПРЕНАТАЛЬНАЯ ДИАГНОСТИКА РЕДКИХ ХРОМОСОМНЫХ ЗАБОЛЕВАНИЙ
Вступление.
По данным Всемирной организации здравоохранения, около 2,5 % новорожденных появляются на свет с разными аномалиями развития. При этом 1,5—2 % из них обусловлены преимущественно неблагоприятными тератогенами, а остальные имеют преимущественно генетическую природу. Среди экзогенных причин пороков развития следует упомянуть биологические (инфекционные заболевания: краснуха, герпес, токсоплазмоз, хламидийная инфекция), физические (все виды ионизирующего излучения, радионуклиды), химические (противоопухолевые препараты, препараты гормональной природы, наркотические вещества).
Основные понятия.
Пренатальная диагностика — это направление современной медицины, представляющее собой процесс выявления или исключения заболеваний плода. Медико-генетическое консультирование помогает ответить на жизненно важные вопросы родителей, касающиеся здоровья будущего ребенка.
На данный момент существует два вида пренатальной диагностики: инвазивная, т. е. предполагает хирургическое вмешательство, и неинвазивная, т. е. без вторжения в полость матки.
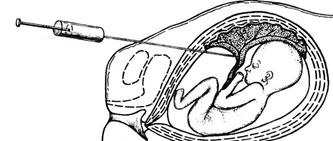
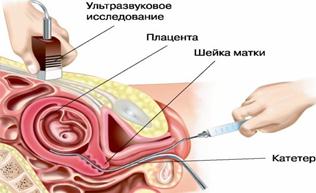
Стоит обратить особое внимание на инвазивные методы исследования: амниоцентез, кордоцентез, биопсия хориона, фетоскопия, плацентоцентез.
1) Амниоцентез. Также возможен влагалищный амниоцентез, но такой подход редко применяется. С амниотической полости забирают 8—10 мл жидкости. С биохимических показателей жидкости только концентрация альфа-фетопротеина (АФП) является диагностически значимой. Уровень АФП существенно повышается при аномалиях нервной трубки и дефектах передней брюшной стенки. Основным источником диагностического материала при амниоцентезе являются клетки. Их обязательно культивируют (это длится 2—4 недели) и для цитогенетических, и для биохимических исследований. Только молекулярно-генетические варианты диагностики с помощью полимеразной цепной реакции не требуют культивирования клеток.
2) Кордоцентез. Обследование проводят в период с 18 по 22 недели беременности. Образцы крови являются объектом для молекулярно-генетических и биохимических методов диагностики наследственных болезней. Кордоцентез используют для диагностики хромосомных болезней, гематологических наследственных болезней: гемоглобинопатии, тромбоцитопении, иммунодефицитов, гематологического статуса при резус-сенсибилизации, внутриутробных инфекций. Преимущество кордоцентеза по сравнению с амниоцентезом заключается в том, что кровь является более удобным объектом для исследования, чем клетки амниотической жидкости. Лимфоциты культивируются быстрее (2—3 дня) и надежнее, чем амниоциты.
3) Фетоскопия (введение зонда и осмотр плода) при современной гибко-оптической технике не является трудновыполнимой. Однако метод используется редко — только при особых показаниях. Работает на 18—23-ей неделе беременности. Практически все врожденные пороки развития, которые можно увидеть с помощью оптического зонда, диагностируются с помощью УЗИ. Понятно, что процедура УЗИ проще и безопаснее. А при фетоскопии выкидыши отмечаются в 7—8 % случаев.
Для этой группы методов необходимы особые показания (возраст матери 35 лет; наличие в семье предыдущего ребенка с хромосомной патологией, в том числе с синдромом Дауна; перестройки родительских хромосом; наличие у семьи заболеваний, которые наследуются, сцеплено с полом; различные наследственные заболевания, диагностируемые методом сцепления с ДНК-маркерами; дефекты нервной трубки.)
Подробнее эти методы рассмотрены в Таблице 1:
Таблица 1.
Методом сцепления с ДНК-маркерами
Метод |
Описание |
Амниоцентез |
Прокол плодного пузыря для получения околоплодной жидкости.
|
Кордоцентез |
Процесс взятия крови из пуповины под контролем УЗИ
|
Фетоскопия |
Введение зонда в амниотическую полость с целью обследования плода для обнаружения врожденных пороков развития
|
Обзор исторических фактов развития цитогенетики:
Следует отметить, что существенную роль в прогрессе цитогенетики человека сыграла новая методика получения метафазных хромосом из культуры лейкоцитов крови in vitro, т. е. «в пробирке», идея которой была высказана еще в 30-х годах отечественным ученым Г.К. Хрущевым. А Ноуэлл, Хангерфорд и Мурхед с сотрудниками разработали метод приготовления препаратов метафазных хромосом из кратковременной культуры ФГА-стимулированных лимфоцитов человека, позволивший существенно упростить получение качественных препаратов для цитогенетического исследования. В 1963 году французские генетики Лежен с соавторами описали первый синдром, связанный с нарушением структуры хромосом. Синдром Лежена или синдром «кошачьего крика». Было выяснено, что частота появления этого порока среди новорожденных около 1:3000. Это и послужило толчком к развитию современной цитогенетики.
Механизм проведения цитогенетического метода.
Предназначение цитогенетического метода заключается в определении кариотипа плода и в выявлении его аномалий. Для этого необходимо получить образец периферической крови. Работа проводится в три этапа:
· Культивирование лимфоцитов крови. Осуществляют стимуляцию деления лимфоцитов, благодаря чему увеличивается количество клеток, находящихся на стадии метафазы. Для остановки деления клеток вводится колхицин. Затем клетки помещают в гипотонический раствор, что приводит к разрушению ядра и выходу хромосом в цитоплазму. Этанол и уксусная кислота фиксируют смесь.
· Далее проводят окрашивание хромосом Q-, R-, C-, G-методами. Методика выбирается в зависимости от цели кариотипирования.
· Заключительным этапом цитогенетического исследования является компьютерный микроскопический анализ.
Особенность проведения метода заключается в том, что один человек анализирует только один кариотип. И также важно, чтобы вовремя кариотипирования специалист очень аккуратно обращался с материалом, т. к. очень сложно достать новый материал. Информация о процессе и результатах анализа строго конфиденциальна.
Выявление хромосомных заболеваний.
Показанием для пренатального кариотипирования является наличие эхографических маркеров ХА у плода, к примеру, увеличенное воротниковое пространство. Единственным методом идентификации хромосомных аббераций является молекулярно-цитогенетический анализ. Упомянем о том, что же такое хромосомные абберации. Это изменения структуры хромосом. Их классифицируют на: делеции или удаление одного из участков хромосомы; инверсии или обратный порядок построения гена; дупликации или повторение участка хромосомы; транслокации или перенос участка с одной хромосомы на другую. Такие хромосомные перестройки нередко приводят к гибели организма. Образование ХА происходит во время кроссинговера, за счет образования разрывов между хромосомами.
Возможности этого метода огромны. Модификации FISH-метода используются при пренатальной диагностике многих хромосомных синдромов: частичных трисомий, моносомий, синдрома Паллистера-Каллиана, микроделеционного синдрома 13q.
Ретроспективный анализ результатов цитогенетической пренатальной диагностики около 300 плодов за 10 лет, при которых показанием к диагностике являлось расширенное воротниковое пространство, показал, что при превышении нормативных значений ВП хромосомные абберации были выявлены у 100 плодов, причем трисомия по 21-й хромосоме была обнаружена в большинстве из них.
Обнаружено, что расширенное воротниковое пространство является фактором риска (учитывая, что в норме толщина воротникового пространства плода не должна превышать 3 мм) т. к. при его наличии у плода резко увеличивается не только частота выявления хромосомных аббераций, но и пороков развития. По статистике у 15 % плодов с расширенным ВП и нормальным кариотипом в дальнейшем выявляются угрожающие жизни пороки развития. Также показано, что обнаружение нарушений сердечно-сосудистой системы у плодов с расширенным ВП выше, чем других патологий.
Таким образом, цитогенетический метод является инновационным методом в исследовании редких хромосомных заболеваний, так как значительная часть множественных врожденных пороков развития и нарушений полового развития, умственной отсталости и отдельных форм злокачественных новообразований, эндокринных и гематологических заболеваний у человека связана с изменением числа или структуры хромосом.
Список литературы:
1. Золотухина Т.В. Пренатальная диагностика хромосомных болезней.
2. Козлова Ю.О., Юдина Е.В., Миньженкова М.Е., Шилова Н.В, Золотухина Т.В. Комплексное обследование плодов с расширенным воротниковым пространством: первый опыт пренатальной диагностики микроделеционных синдромов в клинической практике // Пренатальная диагностика — 2011 — Т. 10, № 1 — С. 47—55.
3. Научный журнал «Медицинская Генетика», 2012 г., № 9.