ИССЛЕДОВАНИЕ ВЛИЯНИЯ ПРЕПАРАТОВ GALLERIA MELLONELLA НА ЭКСПРЕССИЮ НЕЙРОТРОФИЧЕСКИХ ФАКТОРОВ BDNF И NGF
Конференция: LXXXVII Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Секция: Фармакология, клиническая фармакология

LXXXVII Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
ИССЛЕДОВАНИЕ ВЛИЯНИЯ ПРЕПАРАТОВ GALLERIA MELLONELLA НА ЭКСПРЕССИЮ НЕЙРОТРОФИЧЕСКИХ ФАКТОРОВ BDNF И NGF
STUDY OF THE EFFECT OF GALLERIA MELLONELLA PREPARATIONS ON THE EXPRESSION OF NEUROTROPHIC FACTORS BDNF AND NGF
Volchek Igor Anatolyevich
Doctor of Medical Sciences, Professor, Medical Institute of Continuing Education, Federal State Budgetary Educational Institution of Higher Education "Russian Biotechnological University (ROSBIOTECH)", Russia, Moscow
Teryaev Andrey Sergeevich
Director of the Research Center for Immunology and Allergology, Russia, Moscow
Аннотация. В работе исследована активность препаратов Galleria Mellonella, полученных различными методами, в регуляции экспрессии нейротрофических факторов BDNF и NGF in vitro. Для культивируемых нейроглиальных клеток коры больших полушарий крысы показано, что в концентрации 1 мкг/мл происходит статистически достоверная стимуляция экспрессии как BDNF, так и NGF в 3,9–4,8 раз по сравнению с контролем через 1 и 4 часа после введения препаратов.
Abstract. This study investigated the activity of Galleria Mellonella preparations obtained by various methods in regulating the expression of the neurotrophic factors BDNF and NGF in vitro. Using cultured rat cerebral cortex neuroglial cells, it was shown that at a concentration of 1 μg/ml, statistically significant stimulation of both BDNF and NGF expression occurred, 3,9–4,8 times higher than in controls, 1 and 4 hours after administration.
Ключевые слова: экстракт Galleria Mellonella, экспрессия нейротрофинов, BDNF, NGF.
Keywords: Galleria Mellonella extract, neurotrophin expression, BDNF, NGF.
Актуальность. Нейротрофины представляют собой семейство регуляторных белков нервной ткани. Они синтезируются нейронами и клетками нейроглии и играют важную роль в дифференцировке, поддержании жизнеспособности и обеспечении функционирования как периферических, так и центральных нейронов. Регуляция их активности осуществляется посредством аутокринных и паракринных механизмов.
Нейротрофины контролируют нейрональную дифференцировку, стимулируют ветвление дендритов (арборизацию) и рост аксонов (спрутинг) в направлении клеток-мишеней. В зрелой нервной системе они модулируют как кратковременную синаптическую передачу, так и долговременное потенцирование, тем самым внося вклад в пластичность нервной системы, необходимую для ее нормального функционирования.
Зрелые активные формы BDNF являются стабильными гомодимерами с молекулярной массой приблизительно 28 кД. BDNF способствует росту спинальных сенсорных нейронов, а также выживанию и развитию мотонейронов, сенсорных, ганглионарных, дофаминергических, холинергических и ГАМКергических нейронов. Основными продуцентами BDNF являются клетки нейроглии головного и спинного мозга, а также шванновские клетки, ассоциированные с периферическими мотонейронами.
Исследование и разработка средств профилактики и лечения неврологической патологии, включая регуляцию продукции нейротрофических факторов, представляют собой актуальнейшую проблему современных медико-биологических наук. Одним из быстро развивающихся направлений фармакологии является изучение биологически активных средств, основанных на принципах древней традиционной медицины.
Среди множества традиционных рецептур — продукты пчеловодства. В частности, препараты на основе Galleria Mellonella (восковой моли), привлекают особое внимание специалистов в последние годы.
Тем не менее, в доступных научно-литературных источниках не удалось обнаружить непосредственно данных, подтверждающих нейропротекторные и нейротрофические свойства продуктов жизнедеятельности (ПЖ) Galleria Mellonella в контексте нейрофизиологии. Предшествующие исследования были преимущественно сосредоточены на других аспектах, таких как влияние на стресс, иммунный ответ, получение биологически активных веществ для биотехнологии, синтез меланина и другие биологические эффекты.
Целью настоящей работы явилось сравнительное исследование влияния экстрактов Galleria Mellonella, полученных различными способами на продукцию наиболее изученных нейротрофинов BDNF (brain-derived neurotrophic factor) и NGF (nerve growth factor).
Материалы и методы. В качестве исходного сырья использовали сублимированные личинки Galleria Mellonella. Для экстрагирования материала применяли методы: водно-спиртовой экстракции в циркуляционном экстракторе «Сокслет» (Препарат 1); ускоренной экстракции этанолом ASE (Accelerated solvent extraction) (Препарат 2). Растворы стерилизовали фильтрованием и проводили лиофилизацию.
В работе использовались следующие реагенты: L-глютамин, MEM, F12, DMEM, эмбриональная сыворотка коровы (ICN), сахароза, BSA, SDS, EDTA, NaOH, Na2CO3, Na2HPO4, NaCl, PPO, POPOP, бензамидин, PMSF, BDNF, трис, инсулин, трансферрин, прогестерон, путресцин, Na2SeO3, трифторуксусная кислота, гептафтормасляная кислота, трихлоруксусная кислота, ацетонитрил, полиэтиленимин, D-глюкоза, L-глютамин, апротинин, лейпептин (Sigma, Sigma-Aldrich), CuSO4, параформальдегид, Ca,Na-тартрат, соляная кислота, толуол (Реахим), CaCl2, реактив Фолина (Merck), тритон X-100 (“Ferak Berlin”). Использовалась пластиковая культуральная посуда фирм Nunc и Costar.
Первичную культуру клеток нейроглии получали согласно методике [3]. Крыс линии Sprague-Dowly (15 особей) возраста 1–3 дня забивали с помощью углекислотной асфиксии (15 мин.) и помещали на 1 мин. в 80 % водный раствор этанола. Далее все операции проводили в асептических условиях при температуре 4–7оC. Выделенный мозг помещали в раствор Хэнкса и далее выделяли кору больших полушарий, освобождая ткань от оболочек. Выделенную ткань один раз промывали раствором Хэнкса и переносили в среду MEM/F12 (1:1), содержащую 20 % эмбриональной сыворотки коровы и 2 мМ L-глютамина. Ткань диссоциировали на отдельные клетки механически. Полученную клеточную суспензию один раз промывали средой того же состава с помощью центрифугирования при 200 граммах. Клетки засевали плотностью 200 тыс. клеток/см2 на обработанные поли-L-лизином культуральные флаконы площадью 75 см2. Культивирование клеток проводили в CO2-инкубаторе при 370C в атмосфере, содержащей 5 % CO2 и 95 % воздуха в среде MEM/F12 содержащей 15 % эмбриональной сыворотки коровы, 6 г/л D-глюкозы, 2 мМ L-глютамин, 25 мг/л инсулина, 100 мг/л трансферрина, 20 нМ прогестерон, 100 нМ путресцин и 30 нМ селенит натрия, 100 мкг/мл гентамицина. Культуральную среду меняли каждые 3–4 дня. Пересев клеток проводили после достижения монослоя в соотношении 1:3 (время достижения монослоя 1.5–2 нед.).
Выделение тотальной РНК. Для экспериментов использовали полученные после третьего пересева клетки: плотностью 100 тыс./см2 высевали на обработанные поли-L-лизином 6-луночные культуральные планшеты в указанной культуральной среде. После достижения клетками монослоя культуральную среду заменяли на бессывороточную (указанная среда без эмбриональной сыворотки коровы). После 48 ч. инкубации в среду вводили стерильные растворы (40 мкл) тестируемых экстрактов до конечной концентрации 1 мкг/мл (3 параллели на точку). В качестве контроля вводили равный объем 0,9 % раствора NaCl в воде. Через указанные промежутки времени отбирали культуральную среду, клетки промывали холодным фосфатно-солевым буфером и выделяли тотальную РНК фенол-хлороформным методом с использованием набора YellowSolve (Клоноген, Россия) с использованием методики производителя. Чистоту и концентрацию РНК в полученных образцах проводили спектрофотометрически, и в дальнейших экспериментах использовали образцы с соотношением А260/A280 >1.6.
Для проведения обратной транскрипции отбирали 1 мкг тотальной РНК и проводили реакцию 1 час при 370С в среде, содержащей 8 ед /мл Moloney Murine Leukemia Virus (M-MLV)-обратную транскриптазу, 10 мМ дитиотрейтол, 800 мкМ dNTPs, случайные гексапраймеры (20 мкг/мл) и first-strand buffer (50 мМ Трис-HCl, 75 мМ KCl, 3 мМ MgCl2) в объеме 25 мкл. После последующей инкубации 10 мин. при 70 0С образцы полученной кДНК хранили при -200С. Оценку уровня экспрессии BDNF и NGF мРНК проводили с использованием количественной ПЦР в реальном времени (real-time quantitative PCR, система Mx3000P, Stratagene). Применяли высокоспецифичный dsДНК-связывающий краситель SYBR green I. Реакцию проводили в смеси объемом 25 мкл, содержащей 2 мкл кДНК образца или стандарта, или 2 мкл воды (негативная проба), 250 мкМ смеси дНТФ (дезоксинуклеозидтрифосфаты), 2,5 мМ MgCl2,15 мМ Трис-HCl (pH 8,8), 50 мМ KCl, 0,5 % глицерола, 0,1 % Tween 20, интеркалирующий краситель SYBR Green I, 1 ед Taq ДНК-полимеразу с ингибирующими активность фермента антителами («Синтол», Россия) и по 10 пмоль смысловых и антисмысловых праймеров («Синтол», Россия; табл. 1) при следующих условиях: старт — 5 минут 95 0C, затем 40 циклов, включающих плавление — 30 секунд при 95 0C, отжиг — 30 сек. при 68 0C, элонгация — 30 сек. при 72 0C с детекцией флуоресценции в конце каждого шага элонгации.
Для подтверждения специфичности продуктов амплификации после окончания амплификации образцы охлаждали до 60 0C и через 20 мин. получали кривые плавления нагреванием до 95 0C со скоростью 0.03 0C/сек. с непрерывной детекцией флуоресценции. Для получения калибровочных кривых смесь кДНК образцов последовательно разбавляли водой, свободной от ДНКаз, получали стандартные растворы с известной относительной концентрацией соответствующего продукта. С использованием программного обеспечения производителя определяли номер цикла, соответствующий максимальному ускорению процесса амплификации, получали калибровочную кривую числа данных циклов от относительной концентрации продукта, и определяли относительную концентрацию в неизвестном образце с последующей нормализацией по β-актину. Достоверности различий групповых средних оценивались с помощью дисперсионного анализа (one- way ANOVA).
Таблица 1.
Показатели дисперсионного анализа
|
Ген |
Последовательности праймеров (прямой; обратный) |
|
-Актин |
5'‑CTACAATGAGCTGCGTGTGGC‑3' 5'‑CAGGTCCAGACGCAGGATGGC‑3' |
|
BDNF |
5'‑AGCCTCCTCTGCTCTTTCTGCTGGA‑3' 5'‑CTTTTGTCTATGCCCCTGCAGCCTT‑3' |
|
NGF |
5'‑TCAGTGTGTGGGTTGGAGAT‑3' 5'‑AGCCTGTTTGTCGTCTGTTG‑3' |
Результаты. На диаграммах, представленных рисунками 1 и 2, показаны средние значения групп с учетом стандартной ошибки среднего (Mean+SEM). Обозначения уровней достоверности: **– p<0.01; ***– p<0.001.
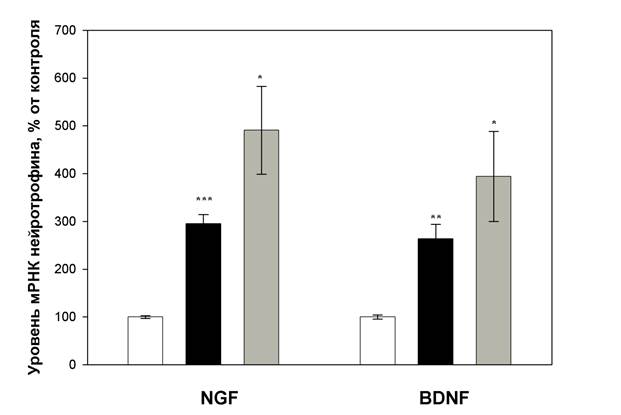
Рисунок 1. Влияние препаратов N1 и N2 в концентрации 1 мкг/мл на экспрессию нейротрофических факторов BDNF и NGF в культивируемых клетках астроцитов коры больших полушарий мозга крысы при инкубации в течение 1 часа. (белый – контроль, черный – препарат N1, серый –, препарат N2; * - p<0.05, ** - p<0.01, *** - p<0.001)
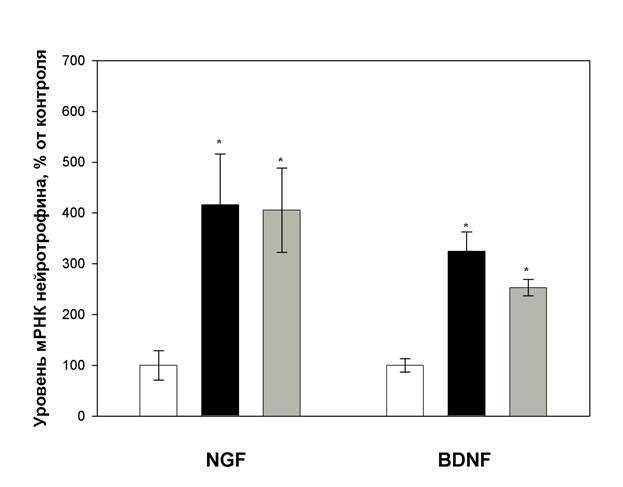
Рисунок 2. Влияние препаратов N1 и N2 в концентрации 1 мкг/мл на экспрессию нейротрофических факторов BDNF и NGF в культивируемых клетках астроцитов коры больших полушарий мозга крысы при инкубации в течение 4 часов. (белый – контроль, черный -препарат N1, серый –, препарат N2; * - p<0.05, ** - p<0.01, *** - p<0.001)
В результате проведенных исследований установлено, что при введении в культуральную среду препарата N1 и препарата N2 в концентрации 1 мкг/мл происходит сильное увеличение экспрессии как BDNF, так и NGF, составляющее 3,9–4,8 раз по сравнению с контролем. Такое увеличение экспрессии является длительным и наблюдается как через 1 час, так и через 4 часа после введения, что показано в вышеприведенных диаграммах (рисунки 1 и 2).
Наиболее значительным и длительным эффектом на увеличение экспрессии BDNF обладал препарат N1. По сравнению с контролем экспрессии BDNF составила 340 % (рисунок 2).
Полученные данные указывают на эффект препаратов Galleria Mellonella в отношении основных нейротрофических факторов BDNF и NGF.
Работы касательно потенциально нейротропного действия экстрактов Galleria Mellonella известны. Так, например, эксперименты с использованием экстрактов личинок Galleria mellonella демонстрировали их стресс-протекторное действие на вегетативном уровне, а также влияние на структуру надпочечников и поведенческие реакции [1; 2].
Однако, как указано выше, конкретные данные о нейропротекторных и нейротрофических механизмах продуктов Galleria Mellonella в доступных источниках ранее нами не были найдены.
Установленный в описываемом в настоящей статье эксперименте факт влияния продуктов восковой моли на метаболизм нейротрофинов, а также всего того, что представляется важным — различия активности препаратов в зависимости от способа получения экстракта — открывает широкие перспективы расширения поиска активных молекулярных комплексов и / или отдельных молекул для коррекции нейродегенеративных процессов.
Кроме того, полученный результат позволяет предполагать обнаружение у исследованных препаратов и антидепрессантной активности, поскольку известно, что прямая инъекция BDNF в гиппокамп лабораторных животных вызывает антидепрессантный эффект [4].
Выводы. В результате проведенных экспериментов показана способность препаратов Galleria Mellonella регулировать экспрессию наиболее изученных нейротрофинов BDNF (brain-derived neurotrophic factor) и NGF (nerve growth factor) в культивируемых астроцитах коры больших полушарий крысы.
Показана связь активности препаратов в зависимости от способа получения экстракта.
Для более глубокого изучения данного вопроса целесообразно проведение дополнительных исследований в области нейробиохимии с перспективой разработки новых биологически активных препаратов.


