Применение полимерных систем, полученных на основе нефтяного порфирина
Конференция: XII Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Секция: Высокомолекулярные соединения

XII Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Применение полимерных систем, полученных на основе нефтяного порфирина
Polymer compositions based on oil porphyrins
Aiganym Ismailova
PhD doctor, lecturer of Kazakh Leading Academy of Architecture and Civil Engineering, Kazakhstan, Almaty
Aigul Zamanbekova
PhD doctor, lecturer of Kazakh Leading Academy of Architecture and Civil Engineering, Kazakhstan, Almaty
Аннотация. Полисахаридные пленки, содержащие хитозан и метилцеллюлоза были получены путем испарения растворителя в и модифицированы нефтяным порфирином. Были изучены взаимодействия химических групп хитозана и метилцеллюлозы до и после щелочной обработки были записаны и проанализированы инфракрасные спектры образцов. Наблюдается исчезновение полос после обработки с NaOH, и возникновение новой полосы ослабления в плоскости NH2 при 1586 см-1 подтверждают превращение ацетата хитозана в форму свободного основания.
С целью оценки возможности химического взаимодействия функциональных групп хитозана, метилцеллюлозы и порфирина были записаны и проанализированы инфракрасные спектры образцов. Результаты показали, что только хитозан эффективно связывается с порфирином, тогда как метилцеллюлоза остается инертной.
Abstract. Polysaccharide films containing chitosan and methyl cellulose were obtained by evaporating the solvent in and modified with oil porphyrin. The interactions of chemical groups of chitosan and methylcellulose before and after alkaline treatment were studied and infrared spectra of the samples were recorded. The bands disappear after treatment with NaOH, and the appearance of a new attenuation band in the NH2 plane at 1586 cm-1 confirm the conversion of chitosan acetate to the free base form.
To assess the possibility of chemical interaction of the functional groups of chitosan, methylcellulose and porphyrin, infrared spectra of the samples were recorded and analyzed. The results showed that only chitosan effectively binds to porphyrin, while methyl cellulose remains inert.
Ключевые слова: нефтяные порфирины; хитозан; метилцеллюлоза; свободные порфириновые основания; ИК – спектры.
Keywords: oil porphyrins; chitosan; methylcellulose; free porphyrin bases; IR spectra.
Важной областью применения нефтяных порфиринов и их аналогов является медицина. Интенсивно развиваются исследования порфиринов в качестве сенсибилизаторов для фотодинамической терапии онкологических заболеваний, основанной на способности порфиринов к накоплению преимущественно в опухолевых клетках и к фотолюмине-сценции с генерацией цитотоксичного синглетного кислорода [1].
Однако, наряду с многими положительными качествами, порфирины обладают кратковременным лечебным действием, что вызывает необходимость его частого введения.
Существующий арсенал онкологических средств в Казахстане невелик и многие из них обладают рядом недостатков, а именно малой продолжительностью противоопухолевого действия, а также токсическим воздействием на организм. Одним из путей устранения этих недостатков является применение принципиально новых полимерных композиционных систем в виде пленок, полученных на основе нефтяных порфиринов.
Среди пленкообразующих полисахаридов хитозан является одним из наиболее широко используемых в фармацевтической промышленности [2-5].
В работе [6] разработаны полимерные композиции на основе нефтяного порфирина и проведен комплекс физико-химических исследований ХТ:МЦ пленок, содержащих порфирин.
С целью оценки возможности взаимодействия химических групп хитозана и метилцеллюлозы до и после щелочной обработки были записаны и проанализированы инфракрасные спектры образцов (рисунок 1).
ИК-полосы на 1540 см-1 (амид II) и 1651 см-1 (амид I) характерны для N- ацетильных групп в хитозане. Соответствующие полосы хитозана были обнаружены при 1376 и 1460 см-1 [7]. Полосы 1034, 1076 и 1152 см-1 возникли из хитозана, а 1063 1110 и 1196 см-1 – из метилцеллюлозы. OH-полосы растяжения хитозана и метилцеллюлозы были обнаружены при 3362 и 3450 см-1 соответственно. Спектр при 3300 см-1 был отнесен к валентным колебаниям хитозана NH. Полосы из метилцеллюлозной пленки при 1372 и 1454 см-1 были отнесены к изгибающим колебаниям СН3.
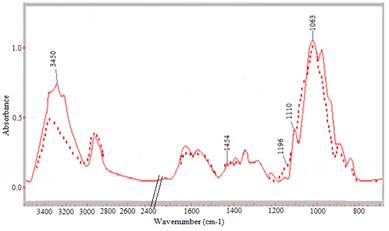
Рисунок 1. ИК-спектры хитозан/метилцеллюлозной пленки: исходные пленки (сплошные) и пленки после щелочной обработки (пунктирные)
Наряду с этим, исчезновение полос после обработки с NaOH, и возникновение новой полосы ослабления в плоскости NH2 при 1586 см-1 подтверждают превращение ацетата хитозана в форму свободного основания.
С целью оценки возможности химического взаимодействия функциональных групп хитозана, метилцеллюлозы и порфирина были записаны и проанализированы инфракрасные спектры образцов (рисунок 2).
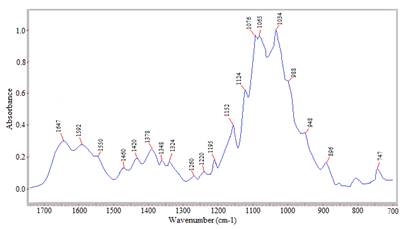
Рисунок 2. ИК-спектры порфириносодержащей биополимерной пленки
Результаты показывают, что только хитозан эффективно связывается с порфирином, тогда как метилцеллюлоза остается инертной.
Полученные данные свидетельствуют о возможности использования полисахаридов хитозана и метилцеллюлозы для создания пленочных лекарственных форм нефтяного порфирина. Установленные закономерности позволяют прогнозировать выход препарата и создавать полимерные материалы с необходимой скоростью поступления порфирина в организм.


