Циклоприсоединение 2-аминофенола к фотоиндуцированным циклическим кетениминам
Конференция: XIV Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Секция: Органическая химия

XIV Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Циклоприсоединение 2-аминофенола к фотоиндуцированным циклическим кетениминам
CYCLOADDITION OF 2-AMINOPHENOL TO PHOTOINDUCED CYCLIC KETENIMINES
Denis Davydov
Student, Lobachevsky State University of Nizhny Novgorod, Russia, Nizhny Novgorod
Andrei Budruev
Associate Professor of the Department of Photochemistry and Spectroscopy, Lobachevsky State University of Nizhny Novgorod, Russia, Nizhny Novgorod
Аннотация. Фотолиз/термолиз арилазида с 2-аминофенолом приводит к образованию конденсированного азепина с молекулярной массой 258 m/z.
Abstract. Photolysis/thermolysis of aryl azide with 2-aminophenol results in the formation of fused azepine with a molecular weight of 258 m/z.
Ключевые слова: ароматический азид; 2-аминофенол; циклоприсоединение; фотохимия.
Keywords: aryl azide; 2-aminophenol; cycloaddition; photochemistry.
В настоящее время активно ведутся работы по поиску новых методов синтеза азагетероциклических соединений, многие из которых проявляют высокую биоактивность и могут применяться в качестве фармпрепаратов. Фотохимический подход во многом облегчает задачу получения данных веществ. Используя УФ-излучение и последующие темновые процессы, можно уменьшить количество стадий реакции. Подобными фоточувствительными соединениями являются ароматические азиды, которые при поглощении кванта света генерируют ряд интермедиатов [1-3], активно участвующих в образовании азагетероциклических соединений [4, 5]. В работе представлены данные циклоприсоединения промежуточных продуктов фотолиза метил 2-азидобензоата (Me2ABK) с 2-аминофенолом (2AP).
Полученные соединения идентифицировали на масс-спектрометре Thermo Electron DSQ II. Инфракрасные спектры (IR) регистрировали на спектрометре Shimadzu IRPrestige-21. Для препаративной колоночной хроматографии использовали Silica gel 60 Merck, элюент – гексан: хлороформ (4: 1, v/v). Продукты фотолиза разделяли методом ВЭЖХ на хроматографе Shimadzu LC-20AD с детектором SPD-M20A, колонкой Discovery C18 d = 3 мм, l = 25 см, скорость потока 0.15 мл×мин‑1.
При интенсивном перемешивании растворы Me2ABK 21.5 мг, 2AP 26.6 мг (2 экв.) и фосфорной кислоты 24.1 мг (2 экв.) в 10 мл смеси этанол-вода, содержащей 20 вес.% воды, облучали в кварцевом реакторе светом ртутно-кварцевой лампы низкого давления БУФ-15 (253.7 нм) в течение 2 часов.
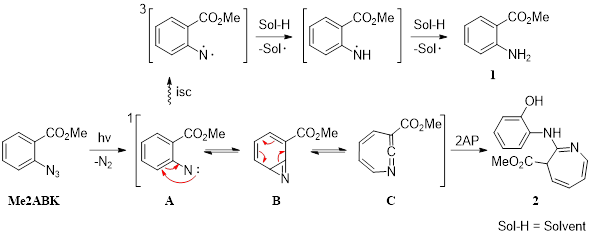
Схема 1. Фотохимическое образование метил 2-аминобензоата 1 и метил 2-((2-гидроксифенил) амино)-3Н-азепин-3-карбоксилата 2
При хроматографическом разделении фотолитической смеси было установлено, что в ходе фотохимической реакции Me2ABK с 2AP образуется два основных продукта. По времени удержания при хроматографическом разделении реакционной смеси и спектру поглощения (Рис. 1b, кривая 1), продукт 1 был идентифицирован как метил 2-аминобензоат. Структура соединения 1 была подтверждена с использованием полученного встречным синтезом этого амина. Продукт 2 идентифицирован как метил 2-((2-гидроксифенил)амино)-3Н-азепин-3-карбоксилат (Схема 1).

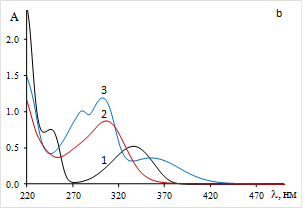
Рисунок 1. Хроматограмма реакционной смеси после фотолиза (  ) и после термолиза (
) и после термолиза (  ) (a), УФ-спектры соединений 1, 2 и 3 (b)
) (a), УФ-спектры соединений 1, 2 и 3 (b)
После добавления 30 мг (6 экв.) гидроксида натрия к фотолитической смеси и ее кипячения с обратным холодильником в течение 1.5 часов происходило превращение вещества 2 с образованием продукта 3. (Рис. 1). Соединение 3 выделено методом препаративной колоночной хроматографии.

Рисунок 2. Масс-спектр соединения 3
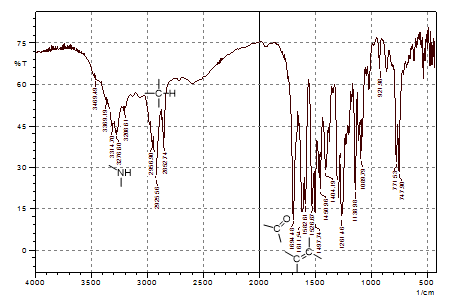
Рисунок 3. ИК-спектр соединения 3
На основании данных масс-спектрометрии установлено, что реакция термолиза соединения 2 идет без потери массы, так как массы веществ 2 и 3 совпадают и равняются 258 m/z (Рис. 2). На ИК-спектре соединения 3 отсутствует полоса поглощения ОН-группы (Рис. 3), что свидетельствует о циклизации 2 по гидроксильной группе. Предполагаемый механизм представлен на схеме 2.

Схема 2. Термоинициированная циклизация соединения 2

