Оптимизация синтеза 5-нитро-4,6-дихлорбензофуроксана с контролем качества исходного сырья, промежуточных и конечных продуктов реакции
Конференция: XVI Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Секция: Фармацевтическая химия, фармакогнозия

XVI Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Оптимизация синтеза 5-нитро-4,6-дихлорбензофуроксана с контролем качества исходного сырья, промежуточных и конечных продуктов реакции
Optimization of the synthesis of 5-nitro-4,6-dichlorobenzofuroxan with quality control of raw materials, intermediate and final reaction products
Albina Mukhametshina
Candidate of Chemical Sciences, Associate Professor, Kazan National Research Technological University, Russia, Kazan
Louise Yusupova
Doctor of Chemical Sciences, Professor, Kazan National Research University of Technology, Russia, Kazan
Ruslan Gilmanov
Doctor of Chemical Sciences, Professor, Kazan National Research University of Technology, Russia, Kazan
Аннотация. 5-нитро-4,6-дихлорбензофуроксан представляет собой биологически активное соединение, обладающее выраженной акарицидной и фунгицидной активностью. В статье приводится оптимизация синтеза 5-нитро-4,6-дихлорбензофуроксана с контролем качества исходного сырья, промежуточных и конечных продуктов реакции.
Abstract. 5-nitro-4,6-dichlorobenzofuroxane is a biologically active compound with a pronounced acaricidal and fungicidal activity. The article presents the optimization of synthesis of 5-nitro-4,6-dichlorobenzofuroxane with quality control of feedstock, intermediate and final reaction products.
Ключевые слова: безофуроксан; биологическая активность; ветеринарный препарат; контроль качества
Keywords: benzofuroxane; biological activity; veterinary drug; quality control
Известно, что 5-нитро-4,6-дихлорбензофуроксан представляет собой биологически активное соединение, обладающее выраженной акарицидной и фунгицидной активностью [1]. Кроме того, он входит в состав ветеринарного препарата «Димиксан» и содержание его в данной композиции составляет 70 %. Инновационный ветеринарный препарат «Димиксан» показал высокую эффективность при лечении грибковых заболеваний кожи животных, демодекоза, вызванного чесоточными клещами вида Psoroptes cuniculi [2]. Препарат прошел доклинические испытания, в результате которых была установлена безопасность его применения. Разработаны лекарственные формы в виде 0,1% водной суспензии для орошения кожного покрова при демодекозе и 0,05% спиртового раствора для лечения отодектоза. Для этих лечебных препаратов установлен 4 класс опасности (LD50= 3500 мг/кг). В связи с этим, для возможности использования 5-нитро-4,6-дихлорбензофуроксана в качестве фармакологически активного ингредиента, необходимо проведение фармацевтической разработки, одним из этапов которой является оптимизация синтеза субстанции 5-нитро-4,6-дихлорбензофуроксана с высоким качеством заданных показателей.
Аналитический образец 5-нитро-4,6-дихлорбензофуроксана представляет собой кристаллический продукт светло-желтого цвета с температурой плавления Тпл. 115-116oС, содержание основного вещества составляет 99,2%. Для выпуска 5-нитро-4,6-дихлорбензофуроксана с заданными показателями, обеспечивающими требуемое качество субстанции, необходимо провести анализ метода синтеза с оценкой рисков, которые могут влиять на показатели качества, а также создания на первом этапе разработки более устойчивой и контролируемой технологии с выбором и оптимизацией контрольных точек, как свойства исходных и промежуточных материалов и параметров процесса.
Синтез 5-нитро-4,6-дихлорбензофуроксана протекает постадийно [3]: 1 – хлорирование 4-нитроанилина; 2 – окисление 2,6-дихлор-4-нитроанилина; 3 – азидирование 2,6-дихлор-4-нитронитрозобензола; 4 – окислительное нитрование 2,6-дихлор-4-азидонитрозобензола; 5 – циклизация 3,5-дихлор-2,4-динитрофенилазида.
На схеме (рисунок 1) представлено: исходное соединение – 4-нитроанилин (1), промежуточные – 2,6-дихлор-4-нитроанилин (2), 2,6-дихлор-4-нитронитрозобензол (3), 2,6-дихлор-4-азидонитрозобензол (4), 3,5-дихлор-2,4-динитрофенилазид (5) и целевой продукт -–5-нитро-4,6-дихлорбензофуроксан (6).
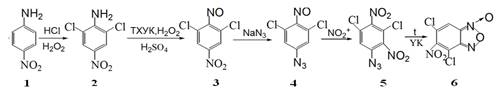
Рисунок 1. Цепь превращений при синтезе 5-нитро-4,6-дихлорбензофуроксана
Контроль качества исходного, промежуточных соединений и целевого продукта осуществлялся с применением физико-химических методов анализа: определение температуры плавлений (Тпл), тонкослойная хроматография (пятна, Rf), инфракрасная спектроскопия (ИК, см-1).
В качестве исходного соединения для синтеза 5-нитро-4,6-дихлорбензо-фуроксана использовали пара-нитроанилин со степенью чистоты «хч». Контроль температуры плавления 4-нитроанилина показал Тпл. =148oС, что полностью совпало с литературными данными [4]. Методом тонкослойной хроматографии установлена индивидуальность соединения и отсутствие примесей. Методом ИК-спектроскопии были идентифицированы основные функциональные группы: 3482 и 3505 см-1 (С-NH2), 1532 см-1 (С-NO2). Таким образом, для синтеза 5-нитро-4,6-дихлорбензофуроксана было взято химически чистое исходное соединение.
Сравнительный анализ известных методов синтеза [5, 6] промежуточного 2,6-дихлор-4-нитроанилина (2) показал, что методом хлорирования соляной кислотой в среде пергидроля [5] продукт реакции получается более чистым, по сравнению с методом, описанным в источнике [6]. Для получения качественного 2,6-дихлор-4-нитроанилина мы провели оценку рисков, которые могут повлиять на качество. При воспроизводстве методики [5], в ходе реакции хлорирования 4‑нитроанилина обнаружили, что помимо 2,6-дихлор-4-нитроанилина образуется 2-хлор-4-нитроанилин, который был идентифицирован методом тонкослойной хроматографии с помощью вещества-свидетеля. Таким образом, по методике, приведенной в литературе, кроме 2,6-дихлор-4-нитроанилина образуется побочный монохлорпродукт. Для достижения чистоты 2,6-дихлор-4-нитроанилина необходима многократная перекристаллизация из этилового спирта.
Для оптимизации стадии хлорирования 4-нитроанилина с целью исключения побочного монохлорпродукта мы варьировали такими параметрами синтеза, как температура и время выдержки. В результате исследований установлены оптимальные параметры стадии хлорирования пара-нитроанилина: выдержка реакции в течение 1-2 часа при 75-80oС. Образовавшийся 2,6-дихлор-4-нитроанилин плавится при температуре 194-195oС. Методом ИК-спектроскопии идентифицировали основные функциональные группы: 1530(С-NO2), 3405 и 3498(С-NH2), 739(С-Cl). Анализ продукта реакции методом ТСХ показал отсутствие монохлорпродукта.
Вторая стадия – окисление 2,6-дихлор-4-нитроанилина (2) до 2,6-дихлор-4-нитронитрозобензола (3) в среде трифторуксусной кислоты – определяет в целом качество конечного целевого 5-нитро-4,6-дихлорбензофуроксана, т. е. является критической. Вместо трифторуксусной кислоты нами была выбрана трихлоруксусная кислота как более дешевый и доступный аналог. Анализ стадии окисления 2,6-дихлор-4-нитроанилина пергидролем в среде трихлоруксусной кислоты при температуре реакции 27-30oС в течение 3 часов показал, что наряду с продуктом 2,6-дихлор-4-нитронитрозобензол остается исходное соединение в виде примеси – 2,6-дихлор-4-нитроанилина, что является крайне недопустимым. Также была проанализирована методика, предложенная авторами [7], по которой синтез 2,6-дихлор-4-нитронитрозобензола осуществлялся при 50oС в течение 15 минут в присутствии пергидроля в среде трихлоруксусной кислоты. Результаты эксперимента показали, что совместно с целевым нитрозонитропродуктом образуется побочное соединение 2,6-дихлор-1,4-динитробензол, что также является крайне недопустимым. Причем последнего количественно больше. Тпл. полученной смеси 154-156oС. Таким образом, исследование реакции окисления 2,6-дихлор-4-нитроанилина в среде трихлоруксусной кислоты показало, что для качества целевого продукта критическими являются температура и время выдержки. При температуре реакции 25-30oС в течение 3 и 4 часов наряду с продуктом реакции - 2,6-дихлор-4-нитронитрозобензолом остается исходное соединение в виде примеси – 2,6-дихлор-4-нитроанилина. При увеличении температуры выдержки (35-40oС) совместно с нитрозопродуктом образуется 2,6-дихлор-1,4-динитробензол, что является недопустимым.
Методом планирования эксперимента установлены оптимальные условиями получения чистого 2,6-дихлор-4-нитронитрозобензола: температура реакции 30-35oС, время выдержки – 3 часа. Целевой продукт очищали перекристаллизацией из водного ацетона. Продукт реакции представляют собой кристаллы белого цвета с оттенком желтизны с Тпл.173-174oС. ИК, см-1: 1544(С-NO2), 1411(С -NО), 734(С-Cl).
Стадия азидирования 2,6-дихлор-4-нитронитрозобензола (3) до 2,6-дихлор-4-азидонитрозобензола водным раствором азида натрия в среде ацетона в условиях по литературной методике [4] протекает без образования побочных продуктов с выходом 90%. Продукт реакции 2,6-дихлор-4-азидонитрозобензол плавится при температуре 139-141 С. ИК, см-1: 1420(С -NО), 735(С- Cl), 2137 (С –N3).
Контроль качества продукта нитрования 2,6-дихлор-4-азидонитрозобензола в условиях литературной методики [6]: азотной кислотой в среде хлороформа при температуре кипения хлороформа показал, что образование побочных продуктов не наблюдается. Выход продукта реакции составил 84%. 3,5-дихлор-2,4-динитрофенилазид (5) очищали методом перекристаллизации из гексана. После однократной перекристаллизации достигали Тпл=114-115oС. ИК, см-1: 1418(С -NО), 738(С-Cl), 1544(С-NO2), 2130 (С –N3).
Реакцию циклизации 3,5-дихлор-2,4-динитрофенилазида осуществляли в среде кипящей уксусной кислоты согласно методике [6]. Нами установлено, что циклизация 3,5-дихлор-2,4-динитрофенилазида протекает без образования побочных соединений. Выход 5-нитро-4,6-дихлорбензофуроксана (6) составил 95%. Тпл=114-115oС. ИК, см-1: 735(С-Cl), 1544(С-NO2), 1630(С=N-O), 1132(N-O). После двукратной перекристаллизации из изопропилового спирта температура плавления составила Тпл=115-116oС.
Таким образом, применение исходного продукта высокого качества, получение промежуточных соединений без примесей и побочных продуктов, а так же строгое соблюдение оптимальных условий синтеза обеспечивает получение 5-нитро-4,6-дихлорбензофуроксана высокой степени чистоты, что является необходимым требованием для получения фармацевтической субстанции.


