ПРИКЛАДНОЕ ЗНАЧЕНИЕ РЕАКЦИЙ ВЗАИМОДЕЙСТВИЯ α-ГАЛОГЕН-β-КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ С 1,3-S,N-НУКЛЕОФИЛАМИ
Журнал: Научный журнал «Студенческий форум» выпуск №31(210)
Рубрика: Химия

Научный журнал «Студенческий форум» выпуск №31(210)
ПРИКЛАДНОЕ ЗНАЧЕНИЕ РЕАКЦИЙ ВЗАИМОДЕЙСТВИЯ α-ГАЛОГЕН-β-КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ С 1,3-S,N-НУКЛЕОФИЛАМИ
Аннотация. Область медицинской химии по праву занимает лидирующее положение в научной отрасли. В современном мире с каждым годом увеличивается количество и вариативность заболеваний, которым подвержено человечество. Самыми распространёнными являются вирусные и раковые заболевания, и одним из современных способов получения новых лекарственных и терапевтических средств являются синтезы с участием S,N-бинуклеофилов с галогенкарбонильными соединениями.
Ключевые слова: вирусные заболевания; противоопухолевый эффект; тиосемикарбазид; тиомочевина; галогенкарбонильные соединения; гетероциклы.
Известно, что при взаимодействии 1,3-S,N-нуклеофилов с карбонильными соединениями конденсируются пяти- и шестичленные гетероциклические циклы. В основных современных способах синтеза применяют как правило тиосемикарбазид, тиомочевину, и другие S,N-бинуклеофильные производные. Результаты трудов в этой области освещены в источниках [1, с. 495], [2, с. 415], [3, с. 1090].
В зависимости от условий протекающей реакции вариативность процесса предполагает получение продуктов конденсации: либо шестичленный 1,3,4-тиадиазиновый цикл, либо пятичленный тиазольный. Вариативность процесса отражена на рисунке 1.
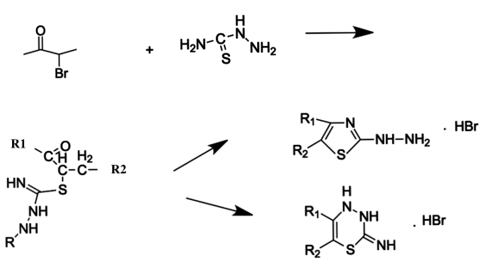
Рисунок 1. Схема взаимодействия 1,3-S,N-нуклеофилов с галогенкарбонильными соединениями
Таким образом, при взаимодействии альфа-галоген-бетта-карбонильных соединений с нуклеофилом типа 1,3-S,N синтезируются гетероциклические соединения, которые в свою очередь либо являются самостоятельно биологически активными элементами, либо являются только промежуточными соединениями для получения более сложных конденсированных биологически активных структур.
Гетероциклические соединения считаются одним из жизненно важных классов органических соединений, которые используются во многих биологических областях, а также при лечении заболеваний. Так, у производных гетероциклических соединений наблюдается высоко значимая биологическая активность: антимикробная, противовоспалительная, противогрибковое, противовирусное, как глистогонное средство, антиоксидантная активность.
Особенное значение приобрёл хороший противоопухолевой эффект.
Гетероциклы были признаны ключевой структурой в медицинской химии, они встречаются в большом проценте биомолекул, таких как ферменты, витамины, натуральные продукты и биологически активные соединения, включая противогрибковые, противосудорожные, противоаллергические, ингибиторы ферментов, анти-ВИЧ, противодиабетические и др.
Так, в последние годы особое внимание уделяется гетероциклическим соединениям, благодаря которым возможно создание лекарственных структур, а также препаратов предупреждающего действия. Самым распространённым и перспективным способом получения вышеупомянутых соединений являются реакции конденсации галоген карбонильных соединений с 1,3-S,N-нуклеофилами.
В настоящее время до сих пор нет эффективных вакцин против вируса гриппа из-за высокой изменчивости вирусов. Однако для лечения вирусной инфекции гриппа были разработаны два вида лекарств: блокаторы ионных каналов и ингибиторы нейраминидазы (NAIs). К сожалению, блокаторы ионных каналов неэффективны из-за резистентности циркулирующих вирусов гриппа А человека, в результате чего NAIs остаются единственными противовирусными средствами, доступными для борьбы с инфекциями гриппа. Исходя из этого положения есть данные [4, с. 3] о том, что две серии новых производных 2-тиазолилгидразона были разработаны и синтезированы с помощью однокомпонентной реакции производных бензальдегида, α-галокетонов и тиосемикарбазида. Все соединения-мишени были оценены на предмет их NA-ингибирующей активности в отношении вирусной нейраминидазы гриппа (H1N1) in vitro, и результаты показали, что многие соединения проявляли умеренную или сильную ингибирующую активность в отношении вирусной нейраминидазы гриппа (H1N1). 2–тиазолилгидразон является эффективным каркасом для ингибиторов NA и что введение этоксикарбонильной группы в 5-положение тиазольного кольца может усиливают ингибирующую активность. Рисунок 2.

Рисунок 2. Схема синтеза 2–тиазолилгидразона
Рак представляет собой важную угрозу общественному здравоохранению, становясь все более распространенным заболеванием во всем мире. Несмотря на многолетние исследования, биохимические процессы, лежащие в основе феномена новообразований, до сих пор до конца не изучены. Особое внимание уделяется взаимодействию между глюкокортикоидами, воспалением и опухолевым процессом. Типичным примером глюкокортикоида является кортизол, который представляет собой гормон, вырабатываемый корой надпочечников. Как острый, так и хронический стресс стимулируют кору надпочечников выделять глюкокортикостероиды, которые приводят к изменениям в ее ежедневной секреции. Они, в свою очередь, влияют на метаболизм белков, углеводов и жиров, а также на течение воспалительных процессов. Адекватная модуляция уровня глюкортикостероидов необходима для правильного функционирования организма.
Иммунная система играет чрезвычайно важную роль во время процесса заболевания, включая образование раковых клеток, например, макрофаги, проявляют стимулирующее воздействие на опухоли посредством множества различных механизмов, включая стимулирование инвазии опухолевых клеток и образования метастазов, стимуляцию ангиогенеза и иммуносупрессивные эффекты. Исследования показали значительную корреляцию между уровнем продуцируемых NK-клеток и экспрессией фермента 11β-HSD1. В ткани, в которой было ≤5% NK-клеток, уровень 11β-HSD1 был значительно выше (приблизительно 45% иммунопозитивных клеток), в то время как в ткани с >5% NK-клеток уровень 11β-HSD1 был значительно ниже (приблизительно 15% иммунопозитивных клеток). Эффективное ингибирование этого фермента способствовало увеличению количества NK-клеток и, следовательно, более сильному ответу со стороны иммунной системы [5, с. 6].
Все полученные производные взаимодействия тиомочевины и производных 2-трет-бутиламинотиазол-4(5Н)-он имеют трет-бутиламинозамещающий элемент во 2-положении, но отличаются в 5-положении тиазольного кольца. Полученные соединения были протестированы in vitro на ингибирование 11β-HSD1 и 11β-HSD2 с целью оценки их избирательного действия и, следовательно, их полезности в качестве потенциальных терапевтических агентов, которые могли бы эффективно поддерживать лечение опухолевых заболеваний. Дальнейшие передовые исследования могут повлиять на понимание патофизиологии этих заболеваний и, следовательно, на использование соответствующих ингибиторов 11β-HSD в терапевтическом процессе. Рисунок 3.
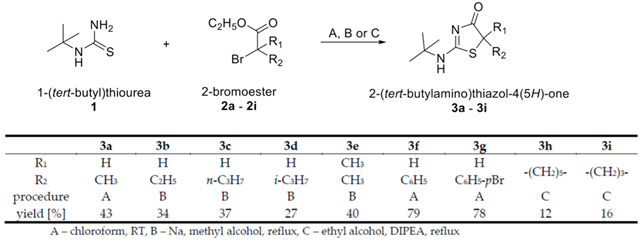
Рисунок 3. Синтез 2-трет-бутиламинотиазол-4(5Н)-она.
Другой способ борьбы с раковыми заболеваниями связан с микротрубочками, как ключевыми компонентами цитоскелета. Они представляют собой цитоскелетные нити, состоящие из гетеродимеров α- и β-тубулина, и играют существенную роль в ряде клеточных процессов, таких как регуляция подвижности, клеточная сигнализация, формирование и поддержание формы клетки, секреция и внутриклеточный транспорт. Из-за важной роли микротрубочек в быстром делении раковых клеток открытие и разработка малых молекул, нацеленных на тубулин, чтобы вмешиваться в динамику тубулина, становится хорошо проверенной стратегией терапии рака [6, с. 3]. Хинолины и их гетероконденсированные каркасы часто встречаются в природных алкалоидах, которые проявляют обширные биологические и фармакологические активности. Аналоги хинолина также проявляют противоопухолевую активность с различными механизмами, включая алкилирующие агенты, ингибиторы тирозинкиназы и ингибиторы тубулина. Среди различных типов активных каркасов хинолинов 2-оксохинолины, класс гетероциклических молекулярных каркасов, получили значительный интерес и внимание из-за их разнообразной фармакологической активности. Арилтиазольные соединения могут нарушать полимеризацию тубулина, тем самым ингибируя образование функциональных микротрубочек и митоз клеток. Рисунок 4.
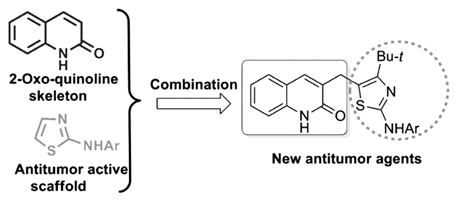
Рисунок 4. Схема синтеза новых противоопухолевых агентов
Чтобы получить такое арилтиазольное соединение, на пятой стадии синтеза участвуют альфа-галлоген-бетта-карбонильное соединение с арилтиомочевиной. Рисунок 5.
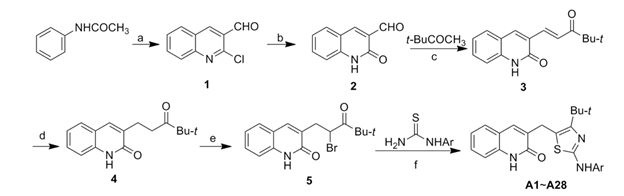
Рисунок 5. Схема синтеза арилтиазольного соединения
Таким образом, реакции взаимодействия α-галоген-β-карбонильных соединений с 1,3-S,N-нуклеофилами представляют собой огромное при создании гетероциклических структур, которые в последствии становятся значимыми агентами в борьбе с самыми распространенными по смертности заболеваниями, такими как вирусные и опухолевые. Из-за высокой биологической активности прикладное значение таких соединений бесконечно и в последующих годах интерес к ним будет возрастать.

