Технология переработки сточных вод производства натриевой соли ДХЦК
Журнал: Научный журнал «Студенческий форум» выпуск №29(50)
Рубрика: Химия

Научный журнал «Студенческий форум» выпуск №29(50)
Технология переработки сточных вод производства натриевой соли ДХЦК
На ТОО «БО-НА» ведется исследования по получение натриевой соли ДХЦК из гипохлорита натрия и циануровой кислоты.
В ходе исследований было проведено моделирование процесса переработки сточных вод в низкосолевой гипохлорит натрия в две стадий хлорирования.
Маточный раствор после разделения содержит от 5 до 13 % NaCl, 1–6 % активного хлора и большое количество воды.
Для переработки этого раствора предлагается хлорирование его с получением низкосолевого гипохлорита натрия и частичного осаждение NaCl.
В непрерывном процессе, на первой стадию к маточному раствору добавляют гидроксид натрия, концентрация щелочи достигает 20 %. После добавление щелочи раствор отправляется на хлорирование, после первого этапа хлорирования концентрация гипохлорита составляет не более 15 %, а щелочи 4,5 %. Так же в процессе хлорирование происходит осаждение хлорида натрия, его концентрация достигает не более 12 %. Раствор охлаждается в теплообменнике.
Выход направляется в кристаллизатор с внешним теплообменником и механической мешалкой. Добавляют дополнительный гидроксид натрия и хлор для получения больших кристаллов хлорида натрия, которые легко фильтруются. Продукт содержит 25 % гипохлорита натрия, 9,5 % хлорида натрия и 0,2–0,8 % гидроксида натрия. Аналогичным способом можно добавлять воду, чтобы получить раствор с 13 % гипохлоритом натрия и 3,5 % хлоридом натрия.
Реакторы были также разработаны, чтобы отделить соль от раствора гипохлорита. Коническое основание вертикальной башни имеет меньший диаметр, чем верхняя часть. Жидкий хлор и раствор гидроксида натрия впрыскивают в нижнюю часть. Гипохлорит удаляется из верхней части колонны, некоторые из которых возвращаются в нижнюю часть Скорость рециркуляции и впрыска контролируют, чтобы кристаллы хлорида натрия псевдоожижались в нижней части реактора, а кристаллы удалялись со дна башни. Кроме того, кристаллы хлорида натрия могут храниться во взвешенном состоянии во всем реакторе и рециркулировать поток. Другой способ предотвращения засорения солей состоит в том, чтобы образовать тонкую пленку раствора гидроксида натрия на стенке реактора ниже своего порта ввода и ввести газ хлора из точки ниже этого порта, которая отделена от стенки реактора. Воздух также вводится вверх в текучий гидроксид. Реактор также может быть спроектирован таким образом, чтобы избежать засорения, как показано на рисунке 5.
Это устройство позволяет избежать охлаждаемых поверхностей, таких как те, которые встречаются с теплообменниками, на которых могут кристаллизоваться компоненты водной смеси. Давление в баке снижается до 0,05 атмосфер, таким образом, вода испаряется, чтобы охладить систему. Вертикальная колонна находится достаточно высоко, так что давление водной смеси составляет около 1 атмосфер в точке, где добавляется хлор. Смесь быстро циркулирует для поддержания суспензии, минимизации роста температуры и предотвращения разложения гипохлорита.
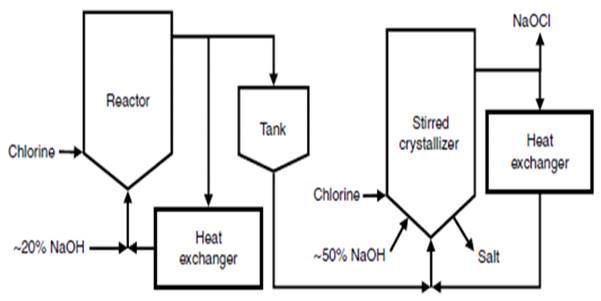
Рисунок 1. Схема производства низкосолевого гипохлорита натрия
Непрерывное удаление соли позволяет получать более высокие концентрации гипохлорита без осаждения пентагидрата гипохлорита натрия. В непрерывном процессе, гидроксид натрия и хлор непрерывно поступает в охлаждаемый реакционный резервуар, в котором степень хлорирования поддерживается выше 80 %. Раствор резервуара циркулирует через центробежный сепаратор для удаления соли и получения раствора с 40,7 % гипохлорита натрия, 2,4 % хлорида натрия и 1,2 % гидроксида натрия.
Данные опыта занесены в таблицу 1 – Результаты хлорирования.
Таблица 1.
Результаты хлорирования
|
Концентрация щелочи перед хлорированием, % |
Концентрация гипохлорита после первой стадий хлорирования, % |
Концентрация щелочи после первой стадий хлорирования, % |
Концентрация гипохлорита после второй стадий хлорирования, % |
Концентрация щелочи после второй стадий хлорирования, % |
|
20 |
15,2 |
4,5 |
25,3 |
0,2 |
|
19,5 |
14,3 |
4,2 |
24,5 |
0,7 |
|
19 |
13,8 |
4,0 |
24,9 |
0,5 |
По таблице 1 был построен график 1 – зависимости концентраций гипохлорита натрия от концентраций щелочи.
На графики 1 видно, что при хлорирование в две стадий максимальная концентрация гипохлорита может достичь 25 %.
При хлорирование в одну стадию максимальное концентрация гипохлорита натрия достигает 15 %, это связано c растворимостью солей в системе 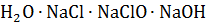 .
.
Для получения гипохлорита натрия высокой концентрации, нужно использовать технологию низкосолевого получения гипохлорита натрия в две стадий хлорирования. Хлорирование щелочи с концентрацией выше 20 % в одну стадию не возможно, т.к. происходит осаждение гипохлорита натрия и хлорида натрия.
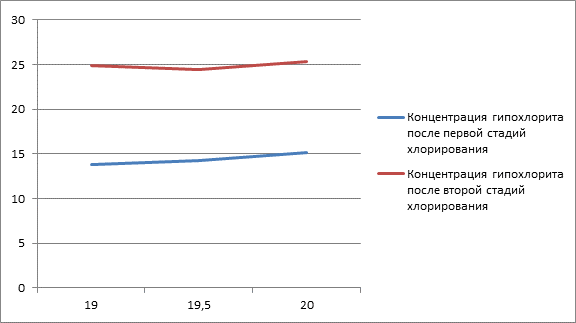
Рисунок 1. зависимость концентрация гпх от концентраций щелочи

