Изучение сорбции ионов меди и цинка на природной и модифицированной глине
Журнал: Научный журнал «Студенческий форум» выпуск №20(156)
Рубрика: Химия

Научный журнал «Студенческий форум» выпуск №20(156)
Изучение сорбции ионов меди и цинка на природной и модифицированной глине
Аннотация. В статье рассмотрено применение природных глинистых минералов в качестве адсорбентов для сорбции тяжелых металлов. Представлены результаты исследований их сорбционной способности по отношению к ионам меди и цинка. Рассмотрен кислотный способ модификации природных глинистых минералов с целью изменения их сорбционной активности. Установлены зависимости величин сорбции от рН. Исследованы адсорбционные модели Ленгмюра и Фрейндлиха.
Ключевые слова: бентонит, монтмориллонит, глины, тяжелые металлы, модификация, сорбция.
Введение
Очистка сточных вод предприятий от тяжелых металлов является одной из главных экологических задач. Преобладающими источниками загрязнения вод являются химические, гальванические и металлургические предприятия. В последние годы увеличиваются сбросы сточных вод промышленных объектов, поэтому технология очистки вод играет значительную роль для человечества [1].
К основным физико-химическим способам очистки сточных вод, подразумевающих собой удаление из них растворенных органических и неорганических веществ, относят:
- коагуляцию;
- экстракцию;
- сорбцию;
- флотацию;
- ионный обмен;
- диализ и др.
Наиболее эффективным методом является сорбционный. Достоинствами данного способа считаются: высокая степень очистки, простота конструкции, хорошая управляемость процессом, отсутствие повторного загрязнения и безопасность.
На данный момент для очистки вод от вредных примесей и ионов тяжелых металлов все чаще используются глинистые минералы. Их широкое применение можно объяснить тем, что они обладают высокой сорбционной активностью, существенной емкостью, химической стойкостью, избирательностью и доступностью [2].
Поглотительная способность природных глинистых пород ограничена и до конца не изучена, поэтому их использование в качестве сорбентов осуществлено не в полной мере. Однако глинистые минералы, обладающие вышеперечисленными свойствами, устанавливающими повышенную адсорбционную способность, указывают на присутствие большого потенциала глин для использования в качестве высокоэффективных сорбентов. Неоднократные исследования монтмориллонит содержащих глин свидетельствуют о возможности их активации и модифицирования путем физического или химического воздействия, которые приводят к изменению адсорбционной емкости. Изменяя условия процесса модифицирования и активации можно получить разные сорбционные материалы с оптимальными характеристиками.
Материалы и методы исследования
В исследовании использовали бентонитовая глина Зырянского месторождения и монтмориллонитовая глина Южно-Оренбургского месторождения.
Средний химический состав бентонитовой и монтмориллонитовой глины представлен в таблице 1[3,4].
Таблица 1.
Химический состав бентонитов и монтмориллонитов
|
Компонент |
Содержание |
|
|
Монтмориллонит |
Бентонит |
|
|
SiO2 |
55,9 |
57,37 |
|
TiO2 |
0,86 |
0,15 |
|
Al2O3 |
18,63 |
19,40 |
|
Fe2O3 |
9,51 |
5,97 |
|
FeO |
- |
0,94 |
|
CaO |
0,72 |
1,81 |
|
MgO |
2,05 |
3,01 |
|
K2O |
3,24 |
1,03 |
|
P2O5 |
- |
0,04 |
|
Na2O |
1,9 |
0,78 |
|
|
- |
0,10 |
|
Ппп |
7,08 |
9,4 |
|
Всего |
99,89 |
100 |
Экспериментальная часть
Объектами исследований являлись: природная бентонитовая и монтмориллонитовая глины, Зырянского и Южно-Оренбургского месторождения соответственно, и их модифицированные образцы, модельные растворы ТМ.
Для приготовления растворов, содержащих ионы металлов, взяты твердые реактивы CuSO4·5H2O (ч.д.а) и ZnSO4·10 H2O (ч.д.а).
Для модифицирования глины обрабатывали соляной кислотой различных концентраций (0,2 М; 2 М; 4 М) при температуре 88 ºC течении двух часов. После глины остужали, промывали несколько раз дистиллированной водой до отрицательной реакции на Cl-. Затем высушивали в течении 12 часов при комнатной температуры, потом в течении 12 часов – при температуре 65 °C до воздушно-сухого состояния [5].
Сорбцию тяжелых металлов из модельных растворов осуществляли при постоянном встряхивании в статическом режиме. Для этого в конические колбы вносили навески сорбентов, растворы с заданными концентрациями сорбатов, выдерживали при перемешивании на колбовстряхивателе при определенном рН. Для поддерживания определенной pH использовали растворы аммиака и серной кислоты. рН раствора при сорбции контролировали с помощью лабораторного иономера И-160-М. Степень сорбционного извлечения (%) определяли по уменьшению содержания ионов металлов до и после сорбции, остаточные концентрации ионов меди и цинка определяли с помощью фотометрических определений с аммиаком и сульфарсазеном соответственно.
Результаты
Установлено, что модифицирование методом кислотной обработки увеличивает сорбционную способность природных глин, так как происходит образование пор в результате растворения полуторных оксидов.
Была исследована зависимость процесса сорбции на глинах при различных pH.
Зависимости степени извлечения сорбции от рН раствора представлены на рисунке 1.
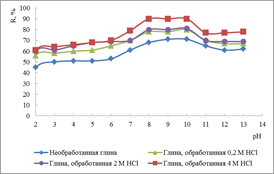
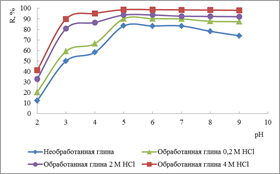
а б
Рисунок 1. Зависимости степени извлечения ионов меди от pH бентонитовой глины (а) и ионов цинка на монтмориллонитовой глине (б)
Наибольшее извлечение ионов тяжелых металлов происходит при использовании глин, обработанных 4 M HCl: Cu2+ – при pH 6 и составляет 90 %, так как в промежутке рН от 5 до 6 наблюдается адсорбция меди без ее осаждения в виде гидроксида, а Zn2+ – при pH 5 и составляет 98,8 %, в связи с тем, что при рН от 5 до 7 цинк находится в ионном состоянии.
По результатам исследования были построены изотермы адсорбции ионов меди и ионов цинка на природной и модифицированной бентонитовой и монтмориллонитовой глинах соответственно (рисунок 2). Вид изотерм адсорбции демонстрируют процесс мономолекулярной адсорбции. Они отражают степень сродства ионов металлов к сорбентам. По изотермам адсорбции определяются некоторые характеристики процесса.
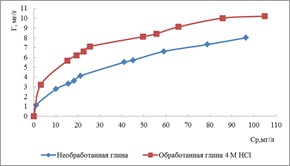
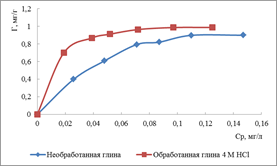
а б
Рисунок 2. Изотермы адсорбции ионов меди на бентонитовой глине (а) и ионов цинка на монтмориллонитовой глине (б)
С помощью уравнения Ленгмюра обработали изотермы адсорбции:
Г=Г∞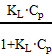 ,
,
в линейной форме:
![]() =
=![]() ,
,
где Г – величина адсорбции, мг/г;
Г∞ – предельная величина адсорбции, мг/г;
KL – константа адсорбционного равновесия;
Cр – равновесная концентрация, мг/л.
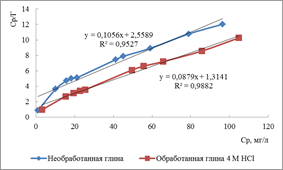
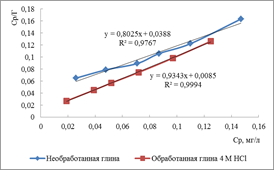
По линейным изотермам Ленгмюра (рисунок 3) графически определили следующие параметры: Г∞ (предельная величина адсорбции) и KL (константа адсорбционного равновесия). Результаты представлены в таблице 2.
а б
Рисунок 3. Изотермы адсорбции в линейных координатах уравнения Ленгмюра ионов меди на бентонитовой глине (а) и ионов цинка на монтмориллонитовой глине (б)
Полученные данные говорят о том, что чем больше значения констант адсорбционного равновесия, тем сильнее проявляются взаимодействия между адсорбентами и адсорбатами.
Для расчетов также используется уравнение Фрейндлиха [6–7]:
Г=![]() ,
,
где Г – величина адсорбции, мг/г;
Cp – равновесная концентрация, мг/л;
KF – константа, равная емкости адсорбента при остаточной концентрации ионов металлов в растворе, равной единице;
n – константа, характеризующая кривизну изотермы в начальной области концентраций [4,5].
Линейные формы изотерм адсорбции Фрейндлиха представлены на рисунке 4, а результаты расчета констант уравнения Фрейндлиха – в таблице 2.
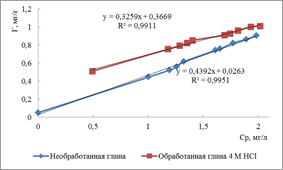
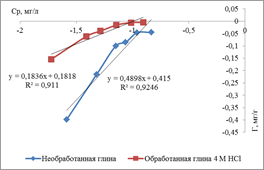
а б
Рисунок 4. Изотермы адсорбции в линейных координатах уравнения Фрейндлиха ионов меди на бентонитовой глине (а) и ионов цинка на монтмориллонитовой глине (б)
Таблица 2.
Параметры адсорбции ионов меди и цинка на бентонитовой и монтмориллонитовой глинах
|
Название глины |
Форма глины |
Модель Ленгмюра |
Модель Фрейндлиха |
||||
|
Г∞, мг/г |
KL |
R2 |
KF |
N |
R2 |
||
|
Бентонитовая глина (излечение Cu2+) |
природная форма |
10,05 |
14,45 |
0,9882 |
1,89 |
2,2 |
0,9951 |
|
H-форма |
11,76 |
15,56 |
0,9527 |
1,25 |
4,03 |
0,9911 |
|
|
Монтмориллонитовая глина (извлечение Zn2+) |
Природная форма |
1,14 |
13,42 |
0,9767 |
1,21 |
2,33 |
0,9246 |
|
Н-форма |
1,33 |
79,09 |
0,9994 |
1,54 |
4 |
0,911 |
|
Благодаря константам уравнения Фрейндлиха можно проводить сравнение активности адсорбционного материала по отношению к тяжелым металлам в различных формах. Из полученных результатов следует, что бентонитовая и монтмориллонитовая глины, которые содержат монтмориллонит в H-форме, являются более активными, чем природная.
Заключение
По результатам исследований установлено, что модифицирование методом кислотной обработки увеличивает сорбционную способность природных глин, это можно объяснить тем, что происходит образование пор в результате растворения полуторных оксидов. Также можно сделать вывод, что глины, обработанные именно 4 М соляной кислотой, обладают более высокими адсорбционными характеристиками по отношению к ионам меди и цинка чем их природные формы.
Наиболее эффективной кислотностью для изучения процесса сорбции меди на бентоните является рН=6, а для сорбции цинка на монтмориллоните - рН=5.
Изотермы адсорбции цинка и меди хорошо описываются моделями Ленгмюра и Фрейндлиха.
Бентонитовая и монтмориллонитовая глины представляют собой наиболее перспективными природными адсорбентами для извлечения ионов меди и цинка из водных растворов.

