ВЛИЯНИЕ ПРИРОДЫ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ НА МОРФОЛОГИЮ И СВОЙСТВА СУСПЕНЗИЙ НА ОСНОВЕ ЗОЛЕЙ КРЕМНИЕВОЙ КИСЛОТЫ
Конференция: LXXX Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Секция: Физическая химия

LXXX Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
ВЛИЯНИЕ ПРИРОДЫ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ НА МОРФОЛОГИЮ И СВОЙСТВА СУСПЕНЗИЙ НА ОСНОВЕ ЗОЛЕЙ КРЕМНИЕВОЙ КИСЛОТЫ
THE EFFECT OF THE NATURE OF ORGANIC SOLVENTS ON THE MORPHOLOGY AND PROPERTIES OF SUSPENSIONS BASED ON SILICA ACIDS
Alevtina Bondareva
Postgraduate student, MIREA – Russian Technological University, Russia, Moscow
Igor Pashkin
Candidate of Science (Chem.), Main expert, MIREA – Russian Technological University, Russia, Moscow
Nadezhda Borisova
Candidate of Science (Chem.), Associate Professor, MIREA – Russian Technological University, Russia, Moscow
Alexander Krylov
Candidate of Science (Chem.), Associate Professor, MIREA – Russian Technological University, Russia, Moscow
В настоящее время широкое распространение для получения прозрачных формоустойчивых гибридных материалов (ГМ) получили процессы золь-гель технологии. Гибридные материалы, полученные с помощью золь-гель процесса, позволяют встраивать органические группы в неорганические системы, объединяя свойства компонентов [5, с. 102]. Оптимизация условий синтеза позволяет создавать ГМ со свойствами, которые являются не только суммой индивидуальных вкладов обеих фаз, но и обладают специфическими и уникальными характеристиками [4, с. 843].
Главное преимущество золь-гель технологии, включающее в себя процессы гидролиза и конденсации, заключается в возможности настройки синтеза путем изменения и мониторинга параметров реакции (например, pH, катализатора, растворителя, температуры и/или концентрации реактантов) [4, с. 843]. Формирование видов с контролируемой наноразмерной архитектурой, уникальной морфологией и свойствами в мягких реакционных условиях обуславливает их широкий спектр применения ГМ в качестве, например, гибридных покрытий, биогибридов и материалов для медицины [13, с. 604].
Число биомедицинских применений гидрогелей стремительно растет благодаря их уникальным физическим, структурным и механическим свойствам. Полимерная сетка внутри жидкости придает гидрогелям уникальные свойства, которые делают их особенно привлекательными для применения в биомедицинской инженерии [9; 10; 13].
Существенное место в биомедицинской инженерии занимают золи и гели кремневой кислоты, которые представляют пористые эластичные материалы с трехмерной полимерной сеткой, поры которых заполнены, в основном, молекулами растворителей или воды, обычно до 70%-99% [9, с. 16071].
Для получения неорганических структур используются, в основном, алкоксисиланы. Тетраэтоксисилаксан (ТЭОС) является одним из наиболее широко используемых прекурсоров для формирования кремнеземной сетки in situ в органической матрице.
Синтез, в основном, состоит из стадии гидролиза алкоксидов кремния, растворенных в исходных спиртах в присутствии минеральных кислот или основного катализатора и последовательных реакций конденсации с участием силанольных групп, в результате которых образуются силоксановые связи и побочные продукты, которыми являются молекулы спирта или воды.
В зависимости от условий гидролиза образование полимера может происходить с различной скоростью. При недостатке воды реакция идет через образование поликремниевых эфиров, которые далее продолжают полимеризоваться с выделением поликремниевой кислоты, в дальнейшем образуя сферические частицы кремнезема, размер которых зависит от условий синтеза.
Морфология конечного продукта, в основном, контролируется типом используемого катализатора. Кислотные реакции, катализируемые кислотами, приводят к образованию трехмерного геля или сетевой структуре [10, с. 267], в то время как реакции, катализируемые основаниями, приводят к образованию конденсированных частиц сферической формы.
Учитывая гетерогенный характер реакции, одним из основных способов управления золь - гель процессом является варьирование соотношения m =H2O/Si для получения конечного продукта желаемого состава и структуры.
Для проведения полного гидролиза тетраалкоксисилана теоретически достаточным является отношение m = 2. Однако даже при избытке воды (m >2) реакция не проходит до конца [4, с. 843]. Вместо этого образуется ряд интермедиатов ([SiOx(OH)y(OR)z]n.
Поскольку алкоксисиланы практически не растворимы в воде в золь-гель технологии часто используют гомогенизирующие водорастворимые растворители – предельные спирты и диолы, ацетон (АЦ), тетрагидрофуран (ТГФ), диоксан (ДО) и др.
Конденсация алкоксисиланолов может проходить как без катализатора, так и в присутствии катализатора по механизму ГТФК и ГМФК и зависит от соотношения m =H2O/Si [8, с. 3060]. Процесс конденсации часто осложняется изменяющейся кислотностью силанольной группы Si-OH алкоксисиланолов (EtO)4-nSi(OH)n при увеличении степени гидролиза [7, с. 889] и влиянием реакций переэтерификации и деполимеризации, которые становятся все более важными с большими концентрациями воды или растворителя.
Известно, что растворители с высокой диэлектрической проницаемостью (e) ускоряют конденсацию силанолов [2, с. 189], однако не наблюдается однозначной корреляции скорости конденсации от e или 1/e растворителей.
Не менее важным является влияние сольватирующей способности растворителя на соотношение стадий гидролиза и конденсации [3, c. 155, c. 12, с. 1239]. Растворитель существенно влияет на механизм ГМФК, что подтверждается данными по конденсации силанолов в среде различных растворителей, при этом происходит изменение механизма процесса. С изменением порядок по силанолу в ацетоне - первый, в диоксане и ДМФА - 3, в ацетонитриле - второй. Чем прочнее комплекс силанола с растворителем, тем труднее происходит замещение растворителя на нуклеофильный реагент.
Время гелеобразования Si(OCH3)4 tg минимально для метанола и формамида (6-8 ч) и значительно увеличивается при переходе к диметилформаамиду и ацетонитрилу (23-20 ч) при нейтральных условиях. Наибольшее время tg наблюдалось для диоксана (41 ч) [1, с. 388].
Золь – гель технология процесса гидролиза ТЭОС в водном растворе или водно – спиртовых средах достаточно изучена и ей посвящено большое количество исследований [4, с. 843; 11, с. 331], в то время как, для других растворителей имеются только отдельные работы.
Добавление органических растворителей в качестве химической добавки для контроля высыхания (Drying Control Chemical Additives) (DCCA) к смеси ТЭОС, воды и спирта улучшает управление структурой и технологичностью золей и гелей при переработке и влияет на морфологию полученной полимерной структуры. Используя эту добавку, можно сушить гели непосредственно в открытом контейнере, избегая процесса растрескивания.
В настоящей работе изучено влияние природы водорастворимых органических соединений, обладающие различной полярностью, донорной и акцепторной способностью - С2Н5ОН, диметилсульфоксида (ДМСО), диметилформамида (ДМФА), ацетонитрила (АН), ТГФ, ДО на морфологию образующихся наноразмерных кремний содержащих частиц (НРЧК) в системах, содержащих 10 - 90 масс% органического растворителя (S). Содержание ТЭОС во всех опытах поддерживалось постоянным и был равным 3 масс.%. Содержание воды в системах с растворителями не превышало 0,5%. Морфология образующихся НРЧК изучена методом динамического светорассеивания (ДЛС).
В результате золь – гель процесса выделяются молекулы С2Н5ОН, и полученная система представляет тройную расслаивающуюся систему Si(OС2Н5)4 + H2O + С2Н5ОН, для которой в области высокого содержания или волы, или спирта или ТЭОС существуют узкие области растворимости кремнезема. Перевод указанной системы в органический растворитель (OS) не только усиливает процессы фазового разделения, но и приводит к высаливанию как ТЭОС, так и НРЧК.
В системах без растворителей (ОS) при высоком содержании H2O (95 – 97 %) тройная система переходит практически в систему Si(OС2Н5)4 + H2O, для которой наблюдается фазовое разделение и практически не наблюдается образования частиц НРЧК в нейтральной среде.
При увеличении содержания ТЭОС до 10-20% заметно увеличивается доля спирта и наблюдается образование двух наборов частиц кремнезема в двух фазовых состояниях. Например, для системы с 10% ТЭОС в фазе, обогащенной водой, средний гидродинамический радиус SiO2 rg <1 нм и во второй фазе, обогащенной С2Н5ОН rg = 23.3 нм (30 %).
По мере увеличения доли ТЭОС до 20 -30 % размеры частиц кремнезема увеличиваются в обеих фазах. Средний гидродинамический радиус SiO2 rg = 8,6 нм и во второй фазе, обогащенной С2Н5ОН rg = 110 нм (рис.1).
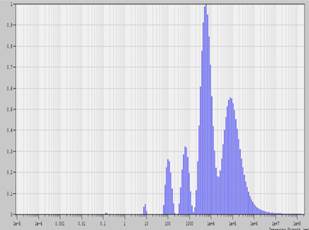
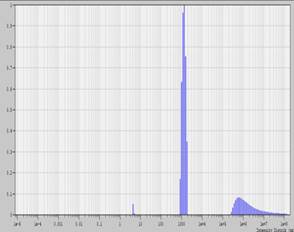
(а) (б)
Рисунок 1. (а) ДЛС спектр системы Si(OС2Н5)4 + H2O в нейтральной среде, (б) ДЛС спектр системы Si(OС2Н5)4 + H2O + АН в нейтральной среде
В области 40 - 60 % ТЭОС размеры фаз выравниваются, и наблюдается выделение крупных частиц поликремневой кислоты.
При дальнейшем увеличении доли ТЭОС до 70% в реакции практически отсутствует H2O, и система переходит к системе Si(OС2Н5)4 + С2Н5ОН, для которой характерны частицы кремнезема среднего размера rg =23 нм.
При дальнейшем увеличении доли ТЭОС до 70-97% происходит полимеризация частиц поликремневой кислоты, и размер rg снова растет до 207 нм, в системе наблюдается обильное выделение в осадок НРЧК.
В системах, обогащенных водой основным продуктом являются частицы поликремневой кислоты, в то время как в системе с большим содержанием С2Н5ОН происходит частичный гидролиз ТЭОС, и образующийся кремнезем сохраняет часть алкоксильных OС2Н5 групп.
В этой связи представляет интерес оценить влияние индифферентных растворителей на направление процесса и структуру образующихся частиц кремнезема.
Введение апротонного растворителя с высокой поляризующей способностью ДМСО (e = 46,68) в систему ТЭОС + H2O приводить к связыванию растворителя с молекулами H2O в прочные ассоциаты (DНсмеш = - 108 кДж/моль), что приводит к уменьшению степени гидролиза ТЭОС. Даже при малом добавление ДМСО к ТЭОС наблюдается микрорасслаивание системы и образование частиц кремнезема размером 46,4 нм. В области 30-40 мол% ДМСО (максимальная доля ассоциатов ДМСО*(H2O)2) наблюдается увеличение НРЧК до rg = 83.1 нм (74,9) %. Дальнейшее рост доли ДМСО приводит к понижению доли НРЧК за счет усиления высаливания ТЭОС, но при этом сохраняется размер частиц rg. Таким образом, размер частиц кремнезема зависит от доли связанной воды и достигает максимального значения в области max содержания ассоциатов ДМСО*(H2O)2.
Диметилформамид является слабоассоциированной жидкостью, водные растворы которого в области высоких концентраций ДМФА состоят, преимущественно, из гетероассоциатов, образованных двумя молекулами ДМФА и одной молекулой воды, а самоассоциаты воды практически отсутствуют (DНсмеш = -272 кДж/моль).
Уменьшение поляризующей способности органического растворителя ДМФА (e= 36,7), по сравнению с ДМСО, приводит к изменению характера микрорасслаивания в системе. Заметное микрорасслаивание системы наблюдается в смесях, содержащих от 10% до 70% ДМФА. В этих условиях наблюдается образование НРЧК размером rg = 50 - 34 нм. При увеличении доли ДМФА выше 80 % не наблюдается микрорасслаивание системы, при этом заметно снижение как средних размеров до rg = 17.3 нм, так и их содержание НРЧК до 6,7 -12%.
Исследование системы ТЭОС + АН + H2O относится к системе, структура растворов которой определяется концентрацией АН.
Несмотря на то, что растворители АН и ДМФА характеризуются практи-чески одинаковыми значениями диэлектрической проницаемостью (e ~ 36), процесс гидролиза ТЭОС в этих растворителях заметно отличается. Принципиальным отличием от ДМСО и ДМФА является наличие микро-гетерогенности водного раствора в широком диапазоне содержания АН (х = 0.1–0.9 м.д.). В интервале х = 0.9–1 структура растворов определяется концентрацией АН, при этом существенная часть воды находится в форме клатратопородобных структур, в которых молекулы воды связаны водородными связями.
Добавление в водный раствор ацетонитрила неорганической или органической соли усиливает фазовое разделение между ацетонитрилом и водой и приводит к высаливание АН [6, стр.971]). Следует отметить, что выделяющийся в реакции этанол также способен вызвать разделение фаз в изначально смешивающемся растворителе с водой.
Образование частиц кремнезема фиксируется как уже при малом, так и при высоком содержании АН в диапазоне rg от 4,26 нм (10 % АН) до 2,38 нм (90% АН). По мере увеличения доли АН растет радиус образующихся микрокапель фазы, богатой АН от 1295 нм (10% АН), 791 нм (20% АН), и при дальнейшем увеличении >70% АН, радиус микрокапель снижается до ~ 300 нм. Таким образом наблюдается прямая зависимость между размером обогащенной водой фазы и размером образующихся НРЧК SiO2. Максимальный размер SiO2 13,45 - 16.6 нм наблюдается в области 40 -70 % АН.
Таким образом, понижение полярности растворителя способствует повышению микрорасслаивания и приводит к образованию частиц кремнезема меньшего размера. Микрофаза, обогащенная водой представляет собой «микрореактор», определяющий размер НРЧК в условиях малого содержания H2O.
Повышение доли воды в системе от 0,5% до 5% приводит к резкому увеличению как содержания SiO2, так и размера частиц кремнезема.
При этом по мере увеличения доли АН растет радиус образующихся микрокапель фазы богатой АН от 264 нм (10% АН), 361,2 нм (20% АН) и до 764 нм (50% АН).
Таким образом, наблюдается прямая зависимость между размером фазы, представляющей собой «микрореактор», и размером образующихся частиц SiO2. Размер частиц SiO2 увеличивается до 102 нм при содержании менее 40% АН, и rg начинают снижаться при концентрациях более 65 % АН, что симбатно изменению размера радиуса капли «микрореактора».
В системе ТЭОС + 20%АН + 5%Н2О доля частиц кремнезема увеличилась до 15,3 % с размерами 57 нм, по сравнению с 2,1% и размером 5,24 нм в системе ТЭОС + 20% АН. При 70% АН размер частиц 45,2 нм (44,3%), при 80% АН размер частиц 28,8 нм (14,2%).
Переход к органическим циклическим эфирам ТГФ и ДО существенно меняет поляризуемость растворителей (e = 7,6 и 2,2 соответственно) и состояние воды в системе. Например, для диоксана и ТГФ характерно микрорасслаивание смесей в широком диапазоне до образования сравнительно крупных самоассоциатов - глобул воды с сеткой водородных связей, и при высоком содержании растворителей продолжается распад водных глобул вплоть до отдельных молекул – тримеров.
Для обоих эфирных растворителей при высоком содержании (S) в системе наблюдается образование НРЧК с rg = 24 - 26,9 нм (67,6%) для ТГФ и rg =55,8 нм (16,8 %) для ДО, и микрорасслаивание с высаливанием ТЭОС в отдельную фазу. При уменьшении доли (S) до х = 10 -20% % системы становится близкими к гомогенной, и размер частиц НРЧК резко возрастает до rg = 114 - 122,4 нм для ТГФ и до 187,0 нм (60,4 %) для ДО.
Таким образом, основными факторами, влияющими на размеры и устойчивость НРЧК являются наличие микрорасслаивания системы, а размер микрокапли -«микрореактора» зависит от характера взаимодействия вода – растворитель.


