Влияние ультразвука на выщелачивание золота йод-иодидными растворителями (по pH и электропроводности)
Конференция: XVIII Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Секция: Физическая химия

XVIII Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Влияние ультразвука на выщелачивание золота йод-иодидными растворителями (по pH и электропроводности)
Аннотация. В работе рассмотрено влияние ультразвука на выщелачивание золота йод-иодидными растворителями (по pH и электропроводности). Описаны роли электропроводности и pH. Уделено внимание зависимостям электропроводности и значений pH от концентрации и времени выщелачивания йод-иодидных растворителей.
Ключевые слова: электропроводность; pH; йод-иодидные растворители; ультразвук; время выщелачивания; золотосодержащие образцы.
Поскольку активность водородных ионов участвует в реакциях с растворенными компонентами и поскольку современные экспериментальные методы позволяют точно определить активность водородного иона, следует всюду, где это возможно, стремиться использовать аН+ как одну из характеристических переменных реакций, с тем, чтобы при сравнении различных реакций существовала бы общая для всех реакций контрольная величина активности. Точно также, ввиду того, что в большинстве случаев активность удобнее всего выражать через логарифмические функции, уже давно был предложен термин pH:
pH=-lg аН+ .
Число реакций, которые могут быть выражены через pH в качестве переменной, весьма значительно. Сюда относятся реакции не только окислов, гидроксилов и основных солей, но также карбонатов, силикатов и сульфидов.
Точно также как для подавляющего большинства реакций можно использовать pH в качестве переменной величины, окислительный потенциал Eh можно использовать для сравнения условий равновесия между различными веществами.
Высокая устойчивость иодидного комплекса золота в широком диапазоне pH и низкая токсичность исходных продуктов в иодидном процессе её, позволяет рассматривать соединение йода перспективной заменой цианиду.
Йодистый калий – бесцветное вещество, по виду его трудно отличить от обычной поваренной соли. Если через водный раствор йодистого калия пропустить ультразвук, то он слегка пожелтеет. Что же произошло? Ричардс и Лумис в 1927 г. обнаружили, что под действием ультразвука молекула йодистого калия, представляющая собой соединение одного атома йода с одним атомом калия, разрушилась, выделился йод, который и окрасил раствор в желтый цвет.
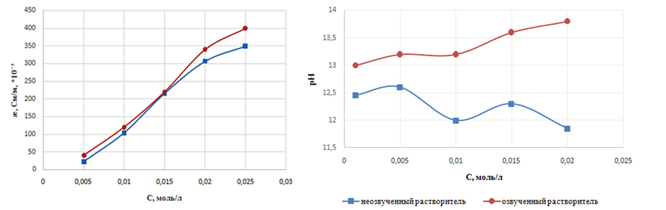
Рисунок 1. Зависимость йод-иодидных растворителей от концентрации а) электропроводности, б) значения pH
Зависимости, представленные на рисунке 1 позволяют сделать некоторые выводы относительно свойств озвученных и неозвученных растворов. На рисунке 1а представлена зависимость электропроводности йод-йодидных растворителей от концентрации.
Из рисунка видно, что облучение ультразвуком ведёт к повышению электропроводности. Причём, электропроводности облучённых и необлучённых ультразвуком растворов при малых концентрациях увеличиваются синхронно и максимально приближаются друг к другу, а при более высоких концентрациях наблюдается резкое увеличение озвученных растворителей.
Одновременно было замечено, что ультразвуковая обработка растворов приводит к увеличению рН, то есть увеличивается концентрация ионов ОН-. На рисунке 1 б изображена зависимость значений рН исследуемых растворов от их концентраций.
Замеры pH и электропроводности показывают, что при воздействии ультразвука на растворы отмечается явление диссоциации молекул.
Также рассмотрим кинетику выщелачивания золота йод-йодидным растворителем. Согласно зависимостям, представленным на рисунках 1а и 2, можно выявить следующие закономерности.
Зависимости изменения электропроводности во времени имеют вид кривых с максимумом, но для разных концентраций максимумы отличаются – острый и пологий. Причём, положение максимума для минимальных концентраций неозвученных растворителей приходится на 170 часов, а для озвученных – на 230 – 250 часов. Для более высоких же концентраций максимум электропроводности для неозвученных растворителей приходится на 90 – 100 часов, а для озвученных это значение составляет 100 – 170 часов. Следует обратить внимание, что при концентрации 0,015 моль/л наблюдается резкое возрастание электропроводности по сравнению с предыдущими концентрациями, то есть в растворе резко увеличивается число ионов. Эта тенденция наблюдается как для озвученных, так и для неозвученных растворителей.
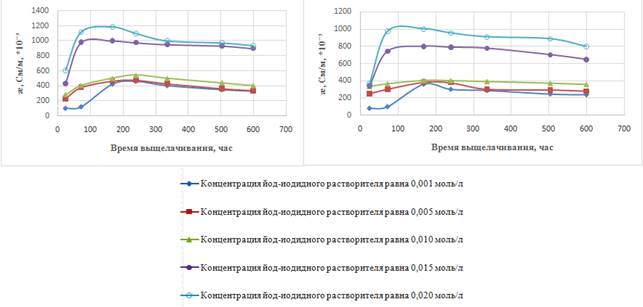
Рисунок 2. Зависимость электропроводности йод-иодидных растворителей от времени выщелачивания а) неозвученных растворителей, б) озвученных растворителей
Анализируя и сравнивая кривые электропроводности, находим, что электропроводность озвученных растворителей выше неозвученных при тех же концентрациях. Например, æ неозвученного растворителя, концентрация которого составляет 0,010 моль/л, составляет 400 См/м, *10-3 при временном промежутке выщелачивания 220 часов, в то время как æ озвученного растворителя при той же концентрации и времени равна 530 См/м, *10-3.
Изучение кинетики электропроводности свидетельствует о том, что во времени в йод-йодидной системе с большой скоростью протекают реакции:
I2 + I- = I3- = I3- + I2 = I5- = 2I3- + I2 = I6- = …
Так как ультразвук способствует выделению молекулярного йода из йодида, то ионов в растворе становится больше и, соответственно, увеличивается электропроводность.
На рисунке 3 показано изменение рН йод-йодидных растворов с течением времени, из которого видно, что рН озвученных растворов изменяется из слабощелочной среды в кислую, причём во времени это происходит в течение первых 7 суток (168 часов), затем ход кривых приобретает плавный характер для всех концентраций.
Для неозвученных растворов изменение рН происходит более плавно из нейтральной среды в кислую до более низких значений по сравнению с озвученными растворителями. То есть, озвучивание растворителей ослабляет общую тенденцию изменения рН (замедляет переход системы в более кислую среду).
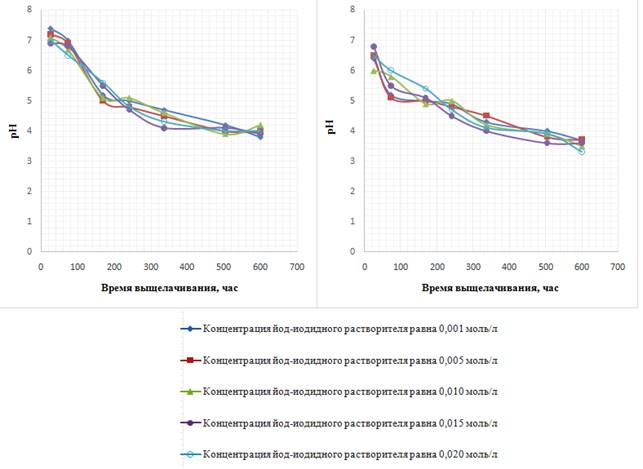
Рисунок 3. Зависимость значения pH йод-иодидных растворителей от времени выщелачивания а) озвученных растворителей б) неозвученных растворителей
Таким образом, можно утверждать, что:
1. Ультразвуковая обработка ведет к снижению времени процесса выщелачивания.
2. Ультразвук способствует увеличению количества извлеченного золота в озвученный раствор на 10-15 % по сравнению с количеством, извлеченным в неозвученный.
3. Облучение ультразвуком ведет к ослаблению тенденции изменения pH.


