Изучение мезопористых носителей на основе кремнезема и алюмосиликата магния методом дифференциальной сканирующей калориметрии
Конференция: XXXIX Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Секция: Фармацевтическая химия, фармакогнозия

XXXIX Международная научно-практическая конференция «Научный форум: медицина, биология и химия»
Изучение мезопористых носителей на основе кремнезема и алюмосиликата магния методом дифференциальной сканирующей калориметрии
STUDY OF MESOPOROUS CARRIERS BASED ON SILICON AND MAGNESIUM ALUMINOSILICATE BY DIFFERENTIAL SCANNING CALORIMETRY
Andrey Filatov
Technologist AMEDART LLC, Russia, Moscow
Zolotov Sergey
production and development director AMEDART LLC, Russia, Moscow
Igor Dain
Chief technologist, PhD in Chemistry, AMEDART LLC, Russia, Moscow
Alexander Cheremisin
Technologist AMEDART LLC, Russia, Moscow
Demina Natalia
Doctor of Pharmacy, Professor, Department of Pharmaceutical Technology, Institute of Pharmacy, First Moscow State Medical University named after I.M. Sechenov (Sechenov University), Russia, Moscow
Аннтотация. Целью данной работы было изучение мезопористых носителей на основе кремнезема и алюмосиликата магния с помшью дифференциальной сканирующей калориметрии (ДСК) при разработке рецептур малорастворимых субстанций. Изученные мезопористые носители могут использоваться для повышения растворимости препаратов БКС класса II и IV группы. Основываясь на данных термограмм носителей был сделан вывод о том, что исследуемые вещества подходят для разработки твердых лекарственных форм с модифицированным высвобождением, в силу сохранения своей аморфной структуры в широком интервале температур.
Abstract. The aim of this work was to study mesoporous carriers based on silica and magnesium aluminosilicate using differential scanning calorimetry (DSC) in the development of formulations for poorly soluble substances. These mesoporous carriers can be used to increase the solubility of BCS class II and IV drugs. Based on the data from the thermograms of the carriers, it was concluded that the investigated substances are suitable for the development of solid dosage forms with modified release, due to the preservation of their amorphous structure in a wide temperature range.
Ключевые слова: мезопористый диоксид кремния; алюмосиликат магния; дифференциальная сканирующая калориметрия.
Keywords: mesoporous silicon dioxide; magnesium aluminum silicate; differential scanning calorimetry.
Введение: АФС (Активная Фармацевтическая Субстанция) в пероральных лекарственных формах необходимо растворить, прежде чем они смогут абсорбироваться в кишечнике и попасть в системный кровоток. Следовательно, как растворение АФС, так и проникновение растворенного АФС через кишечную мембрану в системный кровоток являются важными процессами для достижения необходимой концентрации в крови, чтобы АФС стал эффективным (биодоступность). Высокая скорость растворения АФС в кишечной жидкости может положительно сказываться на скорости проникновения. В 2001 году FDA приняли параметры растворения и проницаемости основными при разработке лекарств, разделяя АФС на 4 класса:
- Высокая растворимость, высокая проницаемость;
- Низкая растворимость, высокая проницаемость;
- Высокая растворимость, низкая проницаемость;
- Низкая растворимость, низкая проницаемость.
Данная система носит название - Биофармацевтическая классификационная система (БКС). Большинство современных АФС относятся ко II и IV классам БКС, имеют низкую растворимость и, как следствие низкую биодоступность [1].
Основным подходом для улучшения растворения и всасывания АФС в кишечнике – является увеличение удельной поверхности частиц АФС микронизация. Для увеличения удельной поверхности частиц используются различные методы микронизации — измельчение, распылительная сушка, наноразмерные субстанции, сокристаллизация, твердые дисперсии, сверхкритическая флюидная технология и другие [2]. Уменьшение размеров частиц этих веществ, как правило, приводит к увеличению скорости растворения и всасывания, повышению биодоступности. Однако, вещества, находящиеся в состоянии сверхтонкого измельчения (микронизированное состояние) термодинамически неустойчивы. При микронизации происходит резкое увеличение удельной поверхности частиц и вместе с тем усиление сил притяжения Ван-дер-Ваальса между молекулами, чтo приводит к процессам агрегации частиц [3].
Для предотвращения или замедления процессов агрегации предложены методы введения лекарственных веществ в твердые носители-матрицы путем их сплавления, растворения (с последующей отгонкой растворителя) или распыление раствора на мезопористые носители.
Для оценки возможности использования изучаемых мезопористых носителей в вышеописанных методах получения ТДС была проведена дифференциальная сканирующая калориметрия.
Материалы и методы: Все образцы мезопористого коллоидного диоксида кремния Syloid 244FP (Syl244), Syloid XDP 3150 (Syl3150), FujiSil (FSL), Parteck SLC (SLC) были получены в виде образцов от WR Grace & Co.-Conn (Колумбия, MR, США), Fuji Chemical Industry Co., Ltd. (Тояма, Япония) и Merck Millipore (Берлингтон, Массачусетс, США), соответственно. Образцы алюмометасиликата магния в форме марок Neusilin US2 (NeuUS2) и Neusilin UFL (NeuUFL) были получены в виде образцов от Fuji Chemical Industry Co., Ltd. (Тояма, Япония).
Дифференциальная сканирующая калориметрия (ДСК) - метод, основанный на регистрации разницы тепловых потоков в зависимости от температуры и времени, что позволяет изучать термические процессы, идентифицировать или сравнивать материалы. Образцы были получены на приборе для дифференциальной сканирующей калориметрии (ДСК) Q20PTA TA Instruments (США). Точно взвешенные 10,0 ± 0,1 мг, мезопористые носители были запечатаны в платиновый поддон, а затем плотно сжаты в закрытом состоянии. Образцы нагревали от 60 до 160 °C со скоростью 10 °C / мин с установленной пустотой второй емкости. Окончательные расчеты и систематизация данных проводились с использованием Microsoft Excel 2016 в операционной системе Microsoft Windows 7. Уровни значимости P <0,05 обозначают значимость во всех случаях [1].
Результаты и обсуждение: Исследуемые носители на основе кремнезема и алюмосиликата магния имеют хорошую термическую устойчивость в диапазоне температур 60 ℃ – 160 ℃, сохраняя свою аморфность. Хотя образцы и имеют разную форму и размер частиц, а также различаются химическим составом, по результатам анализов можно сделать вывод, что все 6 сорбентов-носителей пригодны для разработки твердых лекарственных форм с модифицированным высвобождением. В исследуемых условиях образцы показали фазовую устойчивость и устойчивость к полиморфизму. В технологиях создания твердых дисперсионных систем нам необходимо аморфизировать кристаллические АФС, в то же время нельзя допускать расплавления носителя, что особенно актуально в технологии экструзии горячего расплава. Зная то, как ведут себя носители при нагревании, мы можем подобрать оптимальную технологию производства твердых дисперсионных систем. По этим причинам нам необходимо исследовать устойчивость к нагреванию потенциальных сорбентов [4]. Результаты ДСК показаны на Рисунке 1:
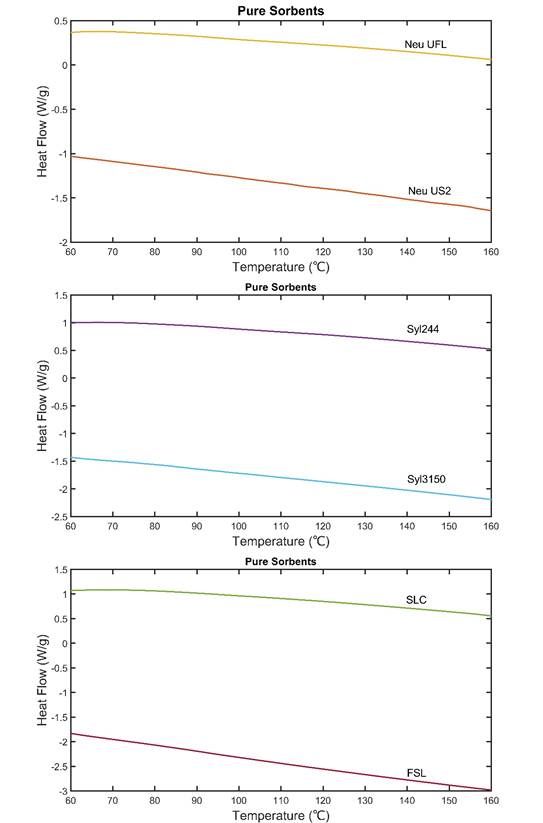
Рисунок 1. ДСК-термограмма носителей

