Особенности нитрования 5,7-дихлорбензофуроксана
Секция: Химия

V Студенческая международная научно-практическая конференция «Естественные и медицинские науки. Студенческий научный форум»
Особенности нитрования 5,7-дихлорбензофуроксана
В настоящее время большое количество исследований проводимых в области современной медицины и синтетической химии направлено на выявление новых биологически активных веществ. Целью этих исследований является получение новых соединений, проявляющих высокую биологическую активность при низких концентрациях. 5,7-дихлорбензофуроксан известен как промежуточное соединение в синтезе галогенопроизводных бензофуроксана. Достоинством этих соединений является то, что они представляют собой биологически активное соединение, проявляют низкую токсичность, высокую акарицидную и бактерицидную активность [1].
Для нитрования 5,7-дихлорбензофуроксана с дальнейшим получением мононитропродукта 4-Н-5,7-ДХБФО перед нами стояла задача выбора нитрующей смеси. Из литературы известно, что некоторые соединения в смеси азотной и серной кислот могут подвергаться гидролизу[1]. Поэтому для получения 4-нитро-5,7-дихлорбензофуроксана задача выбора нитрующей смеси была очень ответственной.
1. Исследование нитрования 5,7-дихлорбензофуроксана азотной кислотой в среде хлороформа;
Для введения одной нитрогруппы, которая вступит в положение 4 бензольного кольца, может быть достаточно нитрование только азотной кислотой. Для исключения возможного гидролиза и создания мягких условий в первую очередь нами исследовано нитрование 5,7-дихлорбензофуроксана азотной кислотой в среде хлороформа по схеме:
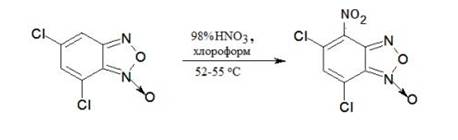
К навеске 1 г 5,7-дихлорбензофуроксана добавили 9,21 мл хлороформа. При температуре не выше 20 ˚С прибавили по каплям 9,21 мл азотной кислоты. Затем реакционную смесь нагревали до 34-36 оС с обратным холодильником в течение 30 мин. После выдержки реакционную массу охладили и разбавили 9,21 мл воды при температуре не выше 60 оС.
Реакционную массу переливали в делительную воронку. Органический слой отделили от водно-кислотного. Органический слой пропустили через бумажный складчатый фильтр, чтобы избавиться от остатков водной кислоты. Органический слой вылили в чашку Петри и упаривали. После полного испарения хлороформа на чашке остаются жёлтые кристаллы 4-нитро-5,7-дихлорбензофуроксана. Выход составил 0,2927 г (24 %), Тпл сырца 87-93˚С. Тпл перекристаллизованного 4-нитро-5,7-дихлорбензофуроксана 100-101˚С Низкий выход, видимо, связан с тем, что часть продукта оставалась в кислотной смеси.
Отсутствие в продукте исходного вещества и образование целевого продукта доказывали методом ТСХ (элюент – гексан:хлороформ 4:1; Rf = 0,28), структуру идентифицировали методом ИК-спектроскопии. ИКС, см-1: 1560 и 1377 (NO2), 1278 (N→O), 1620 (C=N), 1600,1514,1463 (бензольное кольцо), 800-600 (C-Cl). Результаты представлены на рисунках 1 и 2.

Рисунок 1. ТСХ:
№1– 5,7-дихлор-4,6-динитробензофуроксан;
№2– 4-нитро-5,7-дихлорбензофуроксан.

Рисунок 2. ИК-спектр 4-Н-5,7-ДХБФО
2. Исследование нитрования 5,7-дихлорбензофуроксана смесью азотной и уксусной кислот;
Смеси азотной кислоты с уксусной кислотой или с уксусным ангидридом, являющиеся источником ацетилнитрата CH3COONO2, представляют собой относительно мягкие нитрующие агенты, которые применяются для нитрования реакционно способных ароматических или гетероциклических соединений. Их часто применяют в тех случаях, когда действие нитрующей смеси оказывается слишком жестким и приводит к разрушению нитруемого соединения или образованию полинитросоединений. Уксусная кислота и уксусный ангидрид служат в качестве растворителей, а также связывают выделяющуюся в процессе нитрования воду.
С уксусной кислотой азотная кислота не взаимодействует, происходит лишь разрушение димеров азотной кислоты, существование которых было доказано физико-химическими методами, а затем образование комплекса кислота — растворитель за счет водородной связи:
CH3COOH + HNO3 <=> CH3COOH••• HNO3
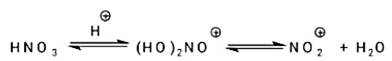
Нитрование смесью азотной и уксусной кислот характеризуется низкой окислительной активностью реагентов, легко регулируется нитрующая активность реагентов, поэтому можно нитровать активированные арены, нитрование в среде уксусной кислоты идёт более селективно и NO2-группа в бензофуроксане преимущественно идёт в 4 положение по схеме:
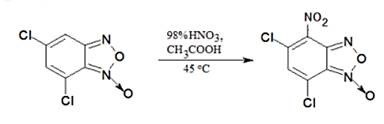
К навеске 1 г (0,004 моль) 5,7-дихлорбензофуроксана добавили 2 мл (0,04 моль) 98 % азотной кислоты и 2 мл (0,04 моль) ледяной уксусной кислоты при перемешивании. Выдерживали в течение 1 часа при постоянном
перемешивании и температуре 58 ˚С. По окончании реакции продукт охлаждали в бане со льдом и разбавили водой и фильтровали. В данном случае, при разбавлении водой продукт осмолялся, образовывалось темно-коричневое вещество. При перекристаллизации выход продукта составляет всего 8-12%.
Было предложено после выдержки реакционную массу перелить в лед. При воспроизведении этого метода, было замечено, что образовывается продукт светло-желтого цвета, с выходом 65%. После перекристаллизации из ИПС, продукт приобретал светло-коричневый цвет, выход составил 34%.
Отсутствие в продукте исходного вещества и образование продукта отслеживали методом ТСХ (элюент – гексан : хлороформ 4:1; Rf = 0,51),идентификацию проводили методом ИК-спектроскопии. ИКС, см-1: 1560 и 1340 (NO2), 1250 (N®O), 1630 (C=N), 1600,1500,1450 (бензольное кольцо), 800-600 (C-Cl).

1 2
Рисунок 3. ТСХ:
№1 – 5,7-ДХБФО; №2 – 4-Н-5,7-ДХБФО
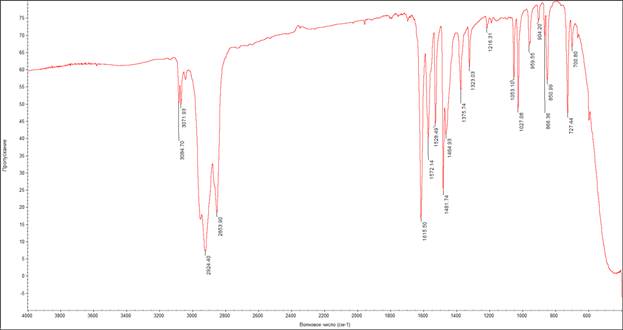
Рисунок 4. ИК-спектр 4-Н-5,7-ДХБФО





